题目内容
【题目】河水含泥沙、细菌等杂质,需要净化处理成自来水。完成自来水厂的生产过程并回答问题:
![]()
(1)为了使沉淀池的悬浮物沉降,通常可加入____
(2)沙滤池可将________过滤除去。
(3)活性炭吸附池的作用是___________
(4)要鉴别自来水是软水还是硬水,可向自来水样品中加入适量的_____,搅拌,如果观察到_____, 则样品为软水。
(5)软化硬水的方法有很多,在日常生活中常用________法。
【答案】明矾 小颗粒不溶物 除色素和异味 肥皂水 泡沫多浮渣少 煮沸
【解析】
(1)为了使沉淀池的悬浮物沉降,通常可加入明矾,是利用明矾在水中形成絮状物质,使悬浮颗粒聚集而沉降;
(2)沙滤池可将沉降还不能除掉的小颗粒不溶物除掉;
(3)活性炭吸附池的作用是通过活性炭的吸附作用,除掉水中的色素和异味;
(4)要鉴别自来水是软水还是硬水,可向自来水样品中加入适量的肥皂水,搅拌,如果观察到泡沫多浮渣少, 则样品为软水;
(5)软化硬水的方法有很多,在日常生活中常用煮沸,可以将硬水中的钙镁化合物转化成沉淀而降低水的硬度。

【题目】某同学用镁条测定空气中氧气含量,实验完毕,冷却后进入水的体积远大于总容积的1/5,且产生了淡黄色固体。某兴趣小组对此现象作如下探究。
(问题)为什么会生成淡黄色固体?为什么测得氧气的体积分数会明显偏大?
(资料)镁元素的化合物的颜色:
物 质 | MgO | MgCl2 | Mg3N2 | Mg(NO3)2 | MgCO3 | Mg(OH)2 |
颜 色 | 白色 | 白色 | 淡黄色 | 白色 | 白色 | 白色 |
(猜想)(1)小组成员一致认为产物中一定不含有氯化镁,理由是_______________。
(2)分析资料,小组成员认为淡黄色固体是Mg3N2,是由镁与空气中的_________(填化学式)反应生成的,导致进入水的体积远大于总容积的1/5。该反应的符号表达式是________。
(实验)小组成员设计并进行了下列实验。

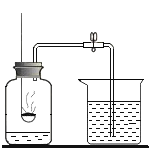
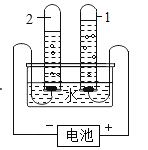
①组装仪器(如下图,钟罩下端无底)。
②将足量白磷在空气中点燃后,迅速伸入钟罩内,塞紧橡皮塞(图1);
③待钟罩内水面不再变化时,向水槽中加水,使水槽中液面与钟罩内液面相平;
④打开橡皮塞,将燃着的螺旋状镁条迅速伸入钟罩内,塞紧橡皮塞(图2);
⑤待钟罩内水面不再变化时,观察到钟罩内壁及表面皿中出现淡黄色固体。
(分析)(3)步骤②中将足量白磷在钟罩内燃烧的目的是__________;钟罩内水面的变化情况_______,
(4)白磷燃烧的符号表达式是_____________。
(5)步骤③中加水的目的是为了防止_______________。
(结论)小组同学的猜想正确。
(拓展)(6)通过以上探究,你对燃烧有什么新认识?请写一点________。