题目内容
(3分)草酸亚铁(FeC2O4)难溶于水,受热会分解。用硫酸亚铁溶液和草酸铵溶液反应可制备草酸亚铁晶体FeC2O4·2H2O(相对分子质量180)。
(1)制草酸亚铁晶体反应的化学方程式 。
(2)18.0gFeC2O4·2H2O加热至400℃,得7.2gFeO、3.6gH2O和 (填序号)。
①CO ②CO2 ③CO和CO2
(1)FeSO4 +(NH4)2C2O4 + 2H2O=FeC2O4·2H2O↓+(NH4)2SO4 (2)③
解析试题分析:(1)依据题意可知:制备草酸亚铁晶体的反应物是硫酸亚铁和草酸铵,生成物之一是FeC2O4·2H2O,另一种生成物可依据反应原理(复分解反应)推出,反应条件为常温,草酸亚铁(FeC2O4)难溶于水,应标出沉淀符号;(2)依据化学式计算18.0gFeC2O4·2H2O碳元素质量为:18.0g× =2.4g;为依据质量守恒定律可得生成气体的质量为:18.0g-7.2g-3.6g=7.2g;若生成的气体为①CO,则含2.4g碳元素需CO质量为:2.4g÷
=2.4g;为依据质量守恒定律可得生成气体的质量为:18.0g-7.2g-3.6g=7.2g;若生成的气体为①CO,则含2.4g碳元素需CO质量为:2.4g÷ =5.6g≠7.2g,假设错误;若生成的气体为②CO2,则含2.4g碳元素需CO2质量为:2.4g÷
=5.6g≠7.2g,假设错误;若生成的气体为②CO2,则含2.4g碳元素需CO2质量为:2.4g÷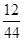 =8.8g≠7.2g,假设错误;5.6g<7.2g,8.8g>7.2g,故生成的气体为③CO和CO2.
=8.8g≠7.2g,假设错误;5.6g<7.2g,8.8g>7.2g,故生成的气体为③CO和CO2.
考点:化学方程式计算;质量守恒定律;平均值法数据分析

 心算口算巧算一课一练系列答案
心算口算巧算一课一练系列答案有铜铝合金8.1g放入300g溶质质量分数为9.8%的稀硫酸中,可能产生氢气的质量是
| A.0.32g | B.0.65g | C.0.84g | D.0.90g |
某不纯的铁5.6g与足量的稀硫酸充分反应,生成0.21g氢气,则铁中混有的金属可能是( )
| A.Zn | B.Cu | C.Mg | D.Ag |
将6.96 g铁的某种氧化物在高温下与足量的一氧化碳充分反应,生成5.28 g二氧化碳,则这种铁的氧化物应该为
| A.FeO | B.Fe2O3 | C.Fe3O4 | D.无法确定 |
小英同学为了测定某地区石灰石样品中碳酸钙的质量分数,取该样品15g,现将75mL的稀盐酸分三次加入石灰石样品中,每次充分反应后测得生成气体的质量,实验数据如下表:
| 实验 | 第一次 | 第二次 | 第三次 |
| 加入稀盐酸的量/mL | 25 | 25 | 25 |
| 生成气体的质量/g | 2.2 | m | 1.1 |
(1)m的值是 g.
(2)求该样品中碳酸钙的质量分数(保留一位小数).
