题目内容
【题目】钙元素是构成人体的重要成分,某补钙药剂的标签主要内容如图所示,现测定该钙片含量是否符合标注,做如下实验:取20片该钙片,放入干燥、洁净的烧杯中,再向烧杯中加入100g某浓度稀盐酸,恰好完全反应(钙片中其他成分不溶于水,也不和稀盐酸反应,反应中产生的气体全部放出),反应后称量烧杯内剩余物质的质量为129g.
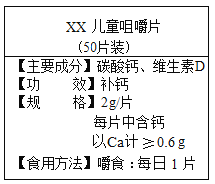
(1)反应中生成二氧化碳质量____g;此反应的基本反应类型为 。
(2)通过计算说明每片钙片实际钙含量是否与标注相符
(3)试计算所用稀盐酸的溶质质量分数.
【答案】11;复分解反应;不符合;18.25%
【解析】
(1)根据质量守恒定律可知,生成二氧化碳的质量为:2g×20+100g-129g=11g,碳酸钙和稀盐酸反应生成氯化钙、水和二氧化碳,该反应是由两种化合物相互交换成分生成两种化合物的反应,属于复分解反应;
(2)设20片钙片中碳酸钙的质量为x,100g盐酸中氯化氢的质量为y。
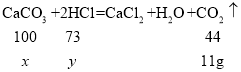
![]() x=25g
x=25g
![]() y=18.25g
y=18.25g
则每片钙片中含钙的质量: ![]() ;
;
0.5g<0.6g,所以不符合;
稀盐酸中溶质的质量分数=![]() 。
。

练习册系列答案
相关题目