题目内容
【题目】金属及其化合物是中学化学学习的重要内容。
(1)《梦溪笔谈》中:“古人以剂刚为刃,柔铁为茎干,不尔则多断折。……”,剂刚、柔铁均为铁的合金,这主要因为合金比纯金属________。
A 硬度大、耐腐蚀 B 硬度小熔点高 C 熔点高、耐腐蚀
(2)某兴趣小组为探究Zn、Fe、Cu、Ag四种金属的活动性,进行下图中甲、乙、丙三个实验。
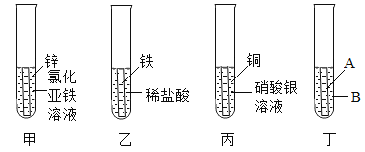
①请写出丙实验中的现象_____________。
②小组同学随后发现该实验无法得出四种金属的活动性顺序,于是补充图丁实验,最终得出四种金属活动性:Zn>Fe>Cu>Ag,则图丁中的试剂A、B分别为__________(写出一组即可)。
(3)某化学实验室从含少量硝酸锌的硝酸银废液中提取金属Ag,其主要操作流程如图:
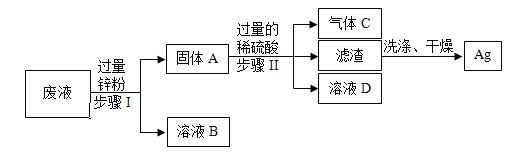
①固体A的成分有________________;
②步骤I、Ⅱ共同的实验操作名称是___________;
③请写出步骤Ⅱ中加入过量稀硫酸的原因__________;若往溶液D中加入适量的铁粉,则发生反应的化学方程式为__________。
(4)2019年诺贝尔化学奖授予三位化学家,以表彰他们在锂离子电池领域的研发工作。利用锂与水的反应可制成锂水电池,作为潜艇的储备电源。已知锂与水反应生成氢氧化锂(LiOH)和一种有可燃性的单质气体,若消耗21g锂,则生成的单质气体质量为多少克________?
【答案】A 铜片表面析出银白色固体,溶液由无色变为蓝色 铜片、稀盐酸 银、锌 过滤 反应掉固体A中的锌,得到银单质 ![]() 3克。
3克。
【解析】
(1)由题意剂刚、柔铁均为铁的合金,这主要因为合金比纯金属熔点低、硬度大、耐腐蚀,A选项正确,符合题意。故选A。
(2)为探究Zn、Fe、Cu、Ag四种金属的活动性,根据图中甲、乙、丙三个实验可知:
甲实验:锌与氯化亚铁溶液反应,实验现象为有黑色单质生成,溶液变为无色;
乙实验:铁表面产生气泡,溶液变为浅绿色;
丙实验:铜片表面析出银白色固体,溶液由无色变为蓝色;
①丙实验中的现象铜片表面析出银白色固体,溶液由无色变为蓝色。
②由以上实验可知金属活动性:Zn>Fe,Cu>Ag,铁能与稀盐酸反应,该实验无法得出四种金属的活动性顺序,要最终得出四种金属活动性为Zn>Fe>Cu>Ag,则补充的丁图的实验要验证铁和铜的金属性强弱,已经有铁和稀盐酸反应的基础上,补充铜与稀盐酸不反应的实验即可证明,则丁图中的试剂A、B分别为铜片、稀盐酸,或者为铜片、硫酸亚铁等。
(3)从含少量硝酸锌的硝酸银废液中提取金属Ag,结合主要操作流程图可知:废液与过量锌粉反应,锌与硝酸银反应生成硝酸锌和银,过滤后得到溶液B硝酸锌溶液和锌、银混合物固体A,锌、银混合物中加入过量稀硫酸,锌与稀硫酸反应生成硫酸锌、氢气,过滤后,溶液D为硫酸、硫酸锌、硝酸锌的混合溶液,滤渣中为银,气体C为氢气,则有:
①固体A的成分有银和锌;
②步骤I、Ⅱ共同的实验操作名称是过滤;
③步骤Ⅱ中加入过量稀硫酸的原因是反应掉固体A中的锌,得到银单质;溶液D为硫酸、硫酸锌、硝酸锌的混合溶液,若往溶液D中加人适量的铁粉,铁与硫酸锌、硝酸锌不反应,铁与稀硫酸反应生成硫酸亚铁和氢气,反应的化学方程式为![]() 。
。
(4)已知锂与水反应生成氢氧化锂(LiOH)和一种有可燃性的单质气体,该气体为氢气,设消耗21g锂,生成的单质气体氢气的质量为x,则有:
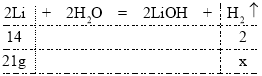
由![]() 解得x=3g
解得x=3g
答:消耗21g锂生成的单质气体氢气的质量为3克。

【题目】某实验小组的同学为了测定实验室中氯酸钾样品的纯度,取一定质量的该样品与1g二氧化锰混合,其总质量为6g.依次加热该混合物t1、t2、t3、t4时间后,分别冷却称量剩余固体质量,记录的有关数据如下表(样品中的杂质不参与化学反应):
加热时间 | t1 | t2 | t3 | t4 |
剩余固体质量/g | 4.24 | 4.16 | 4.08 | 4.08 |
试计算:
(1)完全反应后产生的氧气的总质量为_______。
(2)样品中氯酸钾的纯度是多少_______?
【题目】长期使用的热水锅炉会产生水垢。水垢主要成分是碳酸钙和氢氧化镁。某兴趣小组为了测定水垢中CaCO3的含量,将6g水垢粉碎放在烧杯中,然后向其中加入40g某浓度的稀盐酸,使之充分反应(水垢中除碳酸钙和氢氧化镁外都不与稀盐酸反应)。实验数据记录如下:
反应时间/min | 0 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 |
烧杯内所盛物质的总质量/g | 46.0 | 45.2 | 44.8 | 45.1 | 44.1 | 43.9 | 43.8 | 43.8 | 43.8 |
试计算:
(1)表中有一数据是不合理的,该数据的测得时间是第__________min;
(2)该过程共产生二氧化碳质量为________;
(3)水垢中CaCO3的质量分数________(计算结果精确至0.1%)。