题目内容
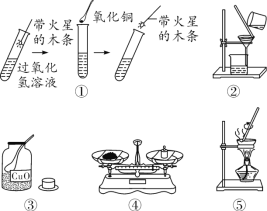
【题目】(2017秦皇岛海港区二模)实验室用过氧化氢溶液制取氧气常用二氧化锰作催化剂,老师提示氧化铜也可以作催化剂。小红做了如图①所示的实验。发现氧化铜确实可以加快过氧化氢的分解。写出小红实验的化学方程式________________。小明认为小红的实验不足以证明氧化铜就是过氧化氢分解反应的催化剂,小明的理由是_____________。
(提出问题)氧化铜在反应前后化性质和质量会改变吗?
(设计并实验)
(1)小红把自己实验后试管中的物质倒入过滤器中进行过滤,如图②所示。发现烧杯的液体中有黑色物质。出现这种现象的原因可能是____________________(答一条即可)。
(2)小红再次过滤后,把滤出的固体加入稀盐酸中,固体消失,溶液慢慢变蓝。小红认为氧化铜在反应前后化学性质没有改变。
小红认为还可以用其他的方法得出同样的结论,她的方法是______________。
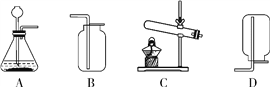
(3)老师在上面实验的基础上又提供了后面③④⑤的实验装置。要想证明氧化铜在化学反应前后质量不发生改变,实验顺序是____________(填序号,装置可重复使用)。
(得出结论)氧化铜是过氧化氢分解反应的催化剂。
(实验反思)
(1)实验过程中小明发现要想把氧化铜全部从滤纸上转移到蒸发皿中几乎不可能,因此严重影响了实验的准确性。为了使实验更准确,他改变了称量方法:___________,解决了这个问题。
(2)实验室为什么不用氧化铜作为过氧化氢分解的催化剂呢?小明猜想二氧化锰的催化效果比氧化铜好。请你帮助小明设计实验证明此猜想:_________。
【答案】![]() 氧化铜的质量和化学性质在化学反应前后是否改变还没有验证 滤纸破损 把滤出的固体再次放入盛有过氧化氢溶液的试管中,立即产生大量气泡 ③④①②⑤④ 称量出湿滤纸和氧化铜的总质量,再称量出一张同样的湿滤纸的质量,两者相减就是氧化铜的质量 将等质量的氧化铜和二氧化锰分别放入等质量、等质量分数的过氧化氢溶液中,观察相同时间内产生气体的快慢
氧化铜的质量和化学性质在化学反应前后是否改变还没有验证 滤纸破损 把滤出的固体再次放入盛有过氧化氢溶液的试管中,立即产生大量气泡 ③④①②⑤④ 称量出湿滤纸和氧化铜的总质量,再称量出一张同样的湿滤纸的质量,两者相减就是氧化铜的质量 将等质量的氧化铜和二氧化锰分别放入等质量、等质量分数的过氧化氢溶液中,观察相同时间内产生气体的快慢
【解析】
注意反应条件要写CuO,2H2O2![]() 2H2O+O2↑;此处考查催化剂的概念,即催化剂的质量和化学性质在化学反应前后没有改变。【设计并实验】(1)经过滤后滤液中仍有黑色物质,可能的原因是:滤纸破损或过滤时滤液高于滤纸。(2)小红是想证明CuO的化学性质在化学反应前后没有改变,所以把滤出的固体再次放入盛有过氧化氢溶液的试管中,若仍然能加快过氧化氢分解的速率,说明其化学性质没变。(3)顺序应为先称量出反应前氧化铜的质量③④,再反应、过滤、干燥①②⑤,再称量出反应后氧化铜的质量④。【实验反思】(1)称量出湿滤纸和氧化铜的总质量,再称量出一张同样的湿滤纸的质量,两者相减就是氧化铜的质量。(2)实验设计的考查通常体现在对比探究和控制变量上,要比较氧化铜和二氧化锰的催化效果,就需要将氧化铜和二氧化锰设置对比,控制其他条件都相同时进行比较。
2H2O+O2↑;此处考查催化剂的概念,即催化剂的质量和化学性质在化学反应前后没有改变。【设计并实验】(1)经过滤后滤液中仍有黑色物质,可能的原因是:滤纸破损或过滤时滤液高于滤纸。(2)小红是想证明CuO的化学性质在化学反应前后没有改变,所以把滤出的固体再次放入盛有过氧化氢溶液的试管中,若仍然能加快过氧化氢分解的速率,说明其化学性质没变。(3)顺序应为先称量出反应前氧化铜的质量③④,再反应、过滤、干燥①②⑤,再称量出反应后氧化铜的质量④。【实验反思】(1)称量出湿滤纸和氧化铜的总质量,再称量出一张同样的湿滤纸的质量,两者相减就是氧化铜的质量。(2)实验设计的考查通常体现在对比探究和控制变量上,要比较氧化铜和二氧化锰的催化效果,就需要将氧化铜和二氧化锰设置对比,控制其他条件都相同时进行比较。

【题目】(2017邯郸二模)某兴趣小组为探究“酒精燃烧的产物”,进行了一系列实验活动,请回答相关问题。
(作出猜想)酒精燃烧的产物有CO2和H2O。
(进行实验)
点燃放置一段时间的酒精灯 | |
实验1 | 将干冷烧杯罩在火焰上方,观察到___,证明有H2O生成 |
实验2 | 用内壁涂有饱和石灰水的小烧杯罩在火焰上方,观察到石灰水___,证明有CO2生成。此反应的化学方程式为_____ |
(反思交流)
(1)甲同学认真分析实验1,认为生成的水可能是由于____,于是做了如下改进实验:点燃刚加入纯酒精的酒精灯,将干冷烧杯罩在酒精灯火焰上方,观察到与实验1相同的现象,证明酒精燃烧有H2O生成。
![]()
(2)乙同学针对实验2提出质疑:石灰水变浑浊不一定是生成碳酸钙,还可能是饱和石灰水受热后__,析出了氢氧化钙固体。于是乙同学做了如图改进实验:6秒后,将锥形瓶加塞子正放在桌面上,待温度恢复至原温时,注入20 mL饱和石灰水振荡,观察到石灰水变浑浊 ,确定有CO2生成。
(3)丙同学观察到棉线灯芯有部分烧黑。由此认为(2)中乙同学的改进实验产生的CO2可能由灯芯棉线燃烧产生的。随后丙同学又做了对比实验:将如图的酒精灯换为盛有纯酒精的____(选填字母:A 量筒 B 集气瓶 C 蒸发皿)后直接点燃,进行实验,仍观察到澄清石灰水变浑浊。证明酒精燃烧有CO2生成。
(得出结论)酒精燃烧的产物有CO2和H2O。
(拓展应用)在验证产物的实验中,应该____(填序号)。
①利用对比法尽量排除其他因素的干扰
②有科学严谨的态度
③注意实验器材的选择
④不考虑那么多的因素,大致看到现象即可