题目内容
【题目】某实验小组用下图所示装置制备常见气体。请回答下列问题:
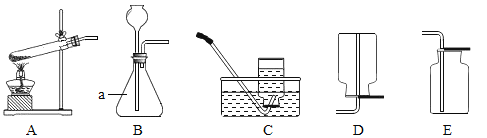
(1)写出图中标号a的仪器名称:____________。
(2)实验小组制取的一种常见气体,既能用C装置收集又能用D装置收集,则选用的发生装置是______(填编号),反应的化学方程式是____________________。
(3)某实验小组用KClO3(MnO2)制取氧气,装置A需要改进的地方是________________。
(4)实验室若用改进后的装置A制取氨气(NH3),应选用的试剂是_______(填序号)。
A.NH4Cl(固体)和Ca(OH)2(固体) B.浓氨水和浓硫酸 C.氯化铵和氢氧化钠溶液
若氨气只能用D装置收集,则氨气_____(填“易”或“不易”)溶于水。
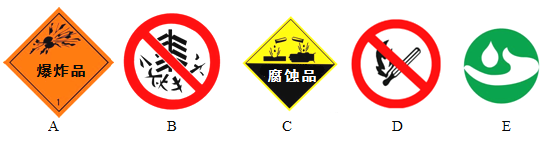
(5)实验小组制取的某气体可用装置E收集,制取该气体的反应方程式是___________(写一条即可)
【答案】锥形瓶 B Zn + H2SO4= ZnSO4+ H2↑ 将试管口略向下倾斜 A 易 CaCO3+ 2HCl =CaCl2+ CO2↑ + H2O(合理即可)
【解析】
(1)a仪器为锥形瓶。
(2)既能用C装置收集又能用D装置收集,说明这种气体不溶于水且密度比空气小,为氢气,实验室常用锌和稀硫酸反应制取氢气,因为反应物是固体和液体,不需加热,所以选择的反应装置为:B;反应的化学方程式是:Zn + H2SO4= ZnSO4+ H2↑。
(3)用KClO3(MnO2)制取氧气反应物是固体,反应条件是加热。加热固体物质试管口要向下倾斜,防止冷凝水回流到试管底部使试管炸裂,故改进措施是:将试管口略向下倾斜。
(4)因为改进后的装置A适用于反应物是固体,反应条件是加热的气体制备,所以用该装置在实验室制取氨气选择的试剂是氯化铵和氢氧化钙的混合物,试剂选项中选A;不能用排水法收集说明氨气易溶于水。
(5)用装置E收集说明这种气体密度比空气大,比如二氧化碳,实验室通常使用碳酸钙和稀盐酸反应来制取,化学方程式是:CaCO3+ 2HCl =CaCl2+ CO2↑ + H2O。

【题目】课题小组为测定某黄铜(铜与锌合金)样品中铜的含量,取20g黄铜样品放在烧杯中,然后向其中分5次注入100g一定浓度的稀盐酸,使之与样品充分反应(杂质不参与反应)。随反应进行,注入稀盐酸的质量与反应剩余固体的质量如下表所示关系。请计算产生氢气的质量___________。(结果保留小数点后一位)
加稀盐酸的次数 | 1 | 2 | 3 | 4 | 5 |
加稀盐酸的质量/g | 20 | 20 | 20 | 20 | 20 |
剩余固体的质量/g | 16.75 | 13.5 | 10.25 | 7 | 7 |