题目内容
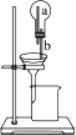
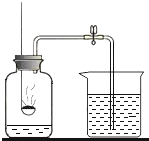
【题目】如图为实验室中常见的气体制备、净化、收集和性质实验的部分仪器。试根据题目要求,回答下列问题:
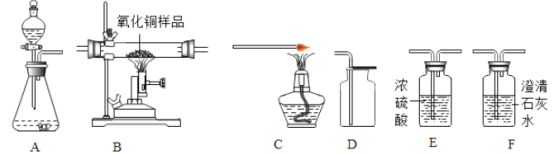
(1)若以石灰石和稀盐酸为原料在实验室中制备并收集干燥的二氧化碳。
①所选仪器的连接顺序为_____(从左到右填写装置序号字母)。
②生成二氧化碳时,所发生反应的化学方程式为_____。
③若将二氧化碳通入澄清石灰水中,石灰水的pH将_____(填“变大”“变小”“不变”之一)。
(2)欲用纯净的一氧化碳气体,测定某不纯氧化铜样品的纯度(CuO+CO![]() Cu+CO2,杂质不反应),并验证气体生成物的性质。某同学所选仪器装置的连接顺序为:纯净的一氧化碳→B→F→C。
Cu+CO2,杂质不反应),并验证气体生成物的性质。某同学所选仪器装置的连接顺序为:纯净的一氧化碳→B→F→C。
①连接仪器装置C的目的是_____。
②若氧化铜样品质量为30g,反应后B装置的质量减少5g,则该氧化铜样品中氧化铜的质量为_____g。
【答案】AED CaCO3+2HCl=CaCl2+CO2↑+H2O 变小 尾气处理,防止污染环境 25g。
【解析】
(1)①实验室制取二氧化碳的反应物是固体和液体,反应条件是常温,浓硫酸具有吸水性,二氧化碳密度比空气大,所以所选仪器的连接顺序为AED;
②碳酸钙和盐酸反应生成氯化钙、水和二氧化碳,化学方程式为:CaCO3+2HCl=CaCl2+CO2↑+H2O;
③氢氧化钙和二氧化碳反应生成碳酸钙沉淀和水,所以将二氧化碳通入澄清石灰水中,石灰水的pH将变小;
(2)①一氧化碳有毒,需要尾气处理,所以连接仪器装置C的目的是:尾气处理,防止污染环境;
②氧化铜和一氧化碳在加热的条件下生成铜和二氧化碳,固体减少的质量就是参加反应的氧元素的质量
设参加反应的氧化铜的质量为x
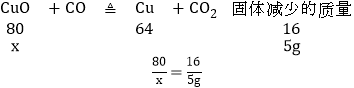
x=25g

练习册系列答案
 口算与应用题卡系列答案
口算与应用题卡系列答案 名师点睛字词句段篇系列答案
名师点睛字词句段篇系列答案
相关题目