题目内容
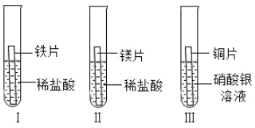
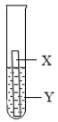
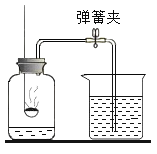
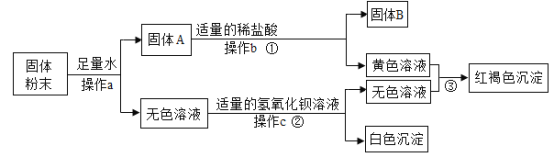
【题目】已知固体混合物A是由KCl、KNO3、BaCO3中的两种或几种组成;另有固体混合物B,已知是由NH4Cl、Mg(NO3)2、CuCl2中的两种或几种组成。按下图所示进行实验,出现的现象如图中所示(设过程中所有发生的反应都恰好完全进行)。
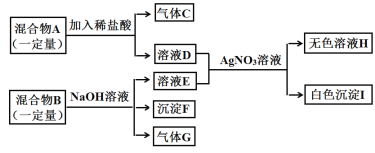
试根据实验过程和发生的现象做出判断,填写以下空白:
(1)气体C和气体G中能使湿润的红色石蕊试纸变蓝的气体是____(写化学式)。
(2)无色溶液H中一定含有的金属阳离子是______。
(3)沉淀F的组成可能有____种(填写数字)。
(4)写出1个生成白色沉淀I的化学方程式______。
(5)混合物B中一定含有______(写化学式)。
(6)混合物A中可能存在的物质是___(写化学式)。如果要确定可能存在的物质,可另取混合物A溶解、过滤,取滤液进行实验,向滤液中滴加___溶液(写化学式),请具体说明实验的现象及结论:__。
【答案】NH3 K+、Na+、Ba2+ 3 AgNO3+ NaCl=AgCl↓ +NaNO3或2AgNO3 +BaCl2=2AgCl↓ +Ba(NO3)2 NH4Cl KCl、KNO3; AgNO3; 若产生白色沉淀则混合物A中一定含KCl,可能含KNO3,若无白色沉淀生成, 则混合物A中一定不含KCl, 一定含KNO3
【解析】
(1)加入稀盐酸后产生的气体B为CO2,加入氢氧化钠后产生的气体为NH3,NH3溶于水显碱性,能使湿润的红色石蕊试纸变蓝;
(2)固体混合物A加盐酸后产生气体,则A中一定有BaCO3,D中一定有生成的氯化钡和原有的氯化钾或硝酸钾中的一种,混合物B加氢氧化钠后产生气体,则B中一定有NH4Cl,E中一定有生成的氯化钠,故D、E与硝酸银混合后所得溶液中一定有的金属阳离子是:K+ 、Na+、 Ba2+;
(3)固体混合物B加入氢氧化钠溶液产生的沉淀可能是氢氧化镁、氢氧化铜,也可能两者都有,故沉淀F的组成可能有3种;
(4)白色沉淀I是AgCl ,由(2)分析知可能是氯化钡和硝酸银反应生成,也可能是氯化钠和硝酸银反应生成,故方程式为2AgNO3 +BaCl2=2AgCl↓ +Ba(NO3)2,AgNO3+ NaCl=AgCl↓ +NaNO3;
(5)混合物B加氢氧化钠后产生气体,则B中一定有NH4Cl;
(6)混合物A加盐酸后产生气体,则A中一定有BaCO3,KCl和KNO3不能确定,故可能有KCl或KNO3;KCl与AgNO3反应生成白色沉淀,可通过加入AgNO3来检验KCl,若加入AgNO3溶液产生白色沉淀,则有一定有KCl,可能有KNO3;若加入AgNO3溶液无白色沉淀生成,则一定无KCl,一定有KNO3,因为固体混合物A是由KCl、KNO3、BaCO3中的两种或几种组成。

 夺冠训练单元期末冲刺100分系列答案
夺冠训练单元期末冲刺100分系列答案 新思维小冠军100分作业本系列答案
新思维小冠军100分作业本系列答案 名师指导一卷通系列答案
名师指导一卷通系列答案【题目】小明家新楼房刚修好。准备用石灰浆刷墙。石灰浆是用生石灰与水充分搅拌形成糊状物。工人师傅将石灰浆糊在墙上推平整。开始墙面很软,慢慢地会自然变干变硬。有一天小明回家,发现刚糊好的墙面掉下一块白色固体。准备通过实验来研究该固体的成分,请你参与。
(猜想)固体可能是A:生石灰,B:_________ ,C:___________。D:熟石灰和石灰石。
小明经过分析认为A是不可能的。请你用方程式解释___________。
(实验)小明取少量固体研细,加入一定量蒸馏水搅拌,澄清。
操作方法 | 现象 | 结论 |
取上层清液少许,滴入1-2滴无色酚酞试液 | 无现象 | 猜想____ 不正确 |
小明另取少量固体于试管,注入___________发现有气泡。故猜想__________成立。
(反思)产生气泡的原因(方程式)______________。
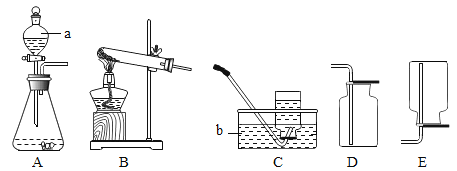
【题目】请根据下列装置回答问题。
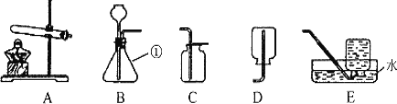
(1)写出图中标号①的仪器名称_____。
(2)实验室用高锰酸钾制氧气的化学方程式为_____, 选择的发生装置是_____(填装置序号,下同),若要收集一瓶供铁丝燃烧实验用的氧气,最适宜选择收集装置是_____。
(3)小组同学为了研究用向上排空气法和排水法收集的氧气浓度是否有差异,做了如下实验:加热高锰酸钾固体,分别用两种方法各收集三瓶氧气,并使用传感器测定收集到的氧气浓度,数据见表。
收集方法 | 向上排空气法 | 排水法 | ||||
氧气浓度/% | 79.6 | 79.7 | 79.9 | 90.0 | 89.8 | 89.3 |
氧气平均浓度/% | 79.7 | 89.7 | ||||
① 用向上排空气法收集氧气时,以能使放置在集气瓶瓶口的带火星木条复燃为氧气集满的标准;用排水法收集氧气时,以观察到_____为氧气集满的标准;
② 向上排空气法收集到的氧气浓度只有 80%左右,下列说法错误的是______填字母序号)。
a.氧气的密度略大于空气的密度,无法将空气排尽
b.加热高锰酸钾固体产生氧气的浓度只有 80%左右
c.当观察到带火星木条复燃时,集气瓶内还有剩余空气
【题目】马英同学取某地石灰石样品12g进行测定实验,现将100g稀盐酸分五次加入石灰石样品中(杂质不溶于水也不参与反应),充分反应后测得生成气体的总质量如表所示:
第1次 | 第2次 | 第3次 | 第4次 | 第5次 | |
加入稀盐酸的质量/g | 20 | 20 | 20 | 20 | 20 |
生成气体的总质量/g | 1.1 | 2.2 | m | 4.4 | 4.4 |
试求:
(1)m的值为_____g。
(2)12g石灰石样品中碳酸钙的质量_____?
(3)所用稀盐酸溶液中溶质的质量分数_____?
(4)反应完全后最终溶液中氯化钙的质量分数_____?(结果保留小数点后一位小数)