题目内容
【题目】某钢铁厂高炉炼铁的主要原料是焦炭、赤铁矿石(主要含Fe2O3)、空气等,主要反应过程如下:
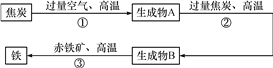
请回答:
(1)A的化学式为________。
(2)反应②的化学方程式为________________;
(3)反应③的化学方程式为________________________。
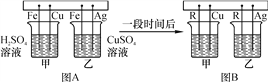
(4)向硝酸银和硝酸铜的混合溶液中,加入一定量的铁粉,反应停止后过滤,得到滤渣和滤液。向滤渣中滴加稀盐酸,无气泡产生,则滤渣中一定含有________(填化学式),滤液中一定含有的溶质是________(填化学式);充分反应后溶液的质量________(填“增大”“减小”或“不变”)。
(5)用含杂质的铁10 g(杂质不溶于水,也不参加反应)与100 g稀硫酸恰好完全反应,滤去杂质,得到滤液质量为108.1 g,求含杂质的铁中铁的质量分数_____________(写出计算过程)。
【答案】 CO2 CO2+C![]() 2CO Fe2O3+3CO
2CO Fe2O3+3CO![]() 2Fe+3CO2 Ag Fe(NO3)2 减小 84%
2Fe+3CO2 Ag Fe(NO3)2 减小 84%
【解析】根据所学知识和题中信息知,(1)A的化学式为CO2,,空气过量。(2)反应②的化学方程式为∶CO2+C![]() 2CO;(3)反应③的化学方程式为∶Fe2O3+3CO
2CO;(3)反应③的化学方程式为∶Fe2O3+3CO![]() 2Fe+3CO2。(4)向硝酸银和硝酸铜的混合溶液中,加入一定量的铁粉,铁比铜,银活泼,铜比银活泼,反应停止后过滤,得到滤渣和滤液。向滤渣中滴加稀盐酸,无气泡产生,铁没有过剩,则滤渣中一定含有Ag,滤液中一定含有的溶质是Fe(NO3)2;充分反应后溶液的质量减小,一个铁置换两个银。
2Fe+3CO2。(4)向硝酸银和硝酸铜的混合溶液中,加入一定量的铁粉,铁比铜,银活泼,铜比银活泼,反应停止后过滤,得到滤渣和滤液。向滤渣中滴加稀盐酸,无气泡产生,铁没有过剩,则滤渣中一定含有Ag,滤液中一定含有的溶质是Fe(NO3)2;充分反应后溶液的质量减小,一个铁置换两个银。
点睛∶碳燃烧氧气充足时生成二氧化碳;不足时生成一氧化碳,或是两者混合物。铁比铜,银活泼,铜比银活泼。

【题目】以下是芳芳小朋友血液中某些元素检测结果的报告单(部分)。
序号 | 检测项目 | 结果 | 参考值 |
1 | 锌 | 7.7 | 11-22 μmol/L |
2 | 铜 | 16.9 | 14-29 μmol/L |
3 | 铁 | 17.8 | 9.0-21.5 μmol/L |
4 | 钙 | 2.0 | 2.2-2.7 μmol/L |
5 | 镁 | 0.84 | 0.8-1.2 μmol/L |
6 | 铅 | 0.28 | 0-0.48 μmol/L |
根据此份报告单并结合自己所学知识回答以下问题:
(1)芳芳缺乏的常量元素是________(填元素符号);芳芳缺乏此元素会________________;检测项目中属于有害元素的是________(填元素符号)。
(2)根据检测结果,医生建议她每天补充10 mg的锌,芳芳的爸爸给她买了下面的补锌剂:

试通过计算说明芳芳每天一共应该吃________片。
(3)芳芳的妈妈认为葡萄糖酸锌片是营养补剂,多吃几片没关系。请你评价这一观点,并说明理由。
______________________________________________