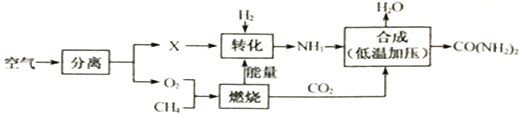
题目内容
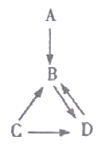
【题目】自来水消毒过程中通常会发生化学反应,其反应的微观过程可用如图表示:
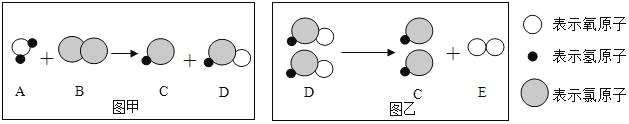
(1)请写出图甲所示反应的化学方程式___
(2)图乙所示反应的基本反应类型为___
(3)B物质属于___(填“单质”或“化合物”),D物质中氯元素的化合价为___,五种物质中属于氧化物的有___(填化学式)
(4)分析以上微观过程模拟图,你能总结出的一条结论是___。
【答案】Cl2+H2O═HCl+HClO 分解反应 单质 +1 H2O 在化学反应中,分子可以再分原子不可再分等
【解析】
(1)由图甲可知,一个氯气分子和一个水分子反应生成一个氯化氢分子和一个次氯酸分子;化学方程式为:Cl2+H2O═HCl+HClO;
(2)由图中可知,反应物是一种,生成物是两种,属于分解反应;
(3)由图中可知,B物质是氯气,是由同种元素组成的纯净物,属于单质;D物质是次氯酸,氢元素是+1价,氧元素是﹣2价,可以求出氯元素的化合价是+1价;由物质的微观构成可知,五种物质中属于氧化物是水,化学式是:H2O;
(4)由微粒的变化可知,在化学反应中,分子可以再分原子不可再分等。

 金钥匙试卷系列答案
金钥匙试卷系列答案【题目】某校化学兴趣小组对苏打(Na2CO3)和小苏打(NaHCO3)在生活中具有何作用、如何鉴别苏打和小苏打进行了如下的探究实验活动,请你参与他们的探究过程,并回答相关问题。
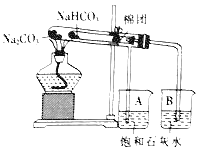
(查阅资料)
信息①相同条件下,碳酸钠溶液的碱性比碳酸氢钠溶的强;
信息②:NaHCO3在270℃时完全分解,会产生一种白色固体以及二氧化碳和水,而Na2CO3不易分解。
(实验过程)
(1)实验一:充分加热后,A、B两个烧杯中分别看到的现象是_____、_____,由此可得出的结论是_____。
(2)实验二:充分利用信息知识,区分无色Na2CO3溶液与NaHCO 3液最简单的方法是_____(填字母)。
A 加热 B 用pH试纸测碱性强弱 C 滴加稀盐酸
(实验反思)
(3)该装置设计的优点是_____。
(4)实验中应注意的问题是_____。
(5)可用小苏打治疗轻度胃酸(主要含盐酸)过多的病人,其原因是_____(用化学方程式进行说明)。
(注意:若答对(实验拓展)奖励4分,化学试卷总分不超过60分。)
(实验拓展)该兴趣小组的同学认为充分加热 NaHCO 3后的白色固体产物可能是NaOH或Na2CO3.请设计实验检验反应后的固体产物,并完成如表。限选试剂及仪器:稀盐酸、氯化钙溶液、澄清石灰水、酚酞溶液、蒸馏水、试管、胶头滴管。
序号 | 实验操作 | 预期现象 | 结论 |
I | 取少量加热后的固体产物于试管A中,加入适量的蒸馏水,充分振荡、溶解,再加入足量的_____,振荡、静置 | 产生白色沉淀 | 产物含Na2CO3 |
Ⅱ | 少量操作后的上层清液于试管B中,滴加_____ | _____ | 产物不含NaOH |