题目内容
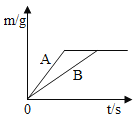
【题目】将等质量的锌粉和铁粉,分别放入质量相等、溶质质量分数相同的稀硫酸中,生成氢气质量(m)随反应时间(t)的变化曲线如图所示,请回答下列问题:
(1)写出锌与稀硫酸反应的化学方程式 _____,
(2)对于该图象的理解,下列说法正确的是_____ (填序号)。
①A表示锌和稀硫酸的反应曲线
②反应结束后两种金属定都有剩余
③反应结束后稀硫酸都没有剩余
④反应结束后消耗两种金属的质量相等
【答案】![]() ①③
①③
【解析】
(1)锌与稀硫酸反应生成硫酸锌和氢气,化学方程式为:![]() ;
;
(2)①.锌的活动性比铁强,所以等质量的金属,锌反应的时间短,正确;
②.由图示可知:生成的氢气的质量相等,所以硫酸均反应完;![]() ,
,![]() ,由方程式分析可知:二者反应结束后,可能金属都有剩余,也可能锌恰好反应完,铁有剩余;故错误;
,由方程式分析可知:二者反应结束后,可能金属都有剩余,也可能锌恰好反应完,铁有剩余;故错误;
③.该置换反应是金属置换酸中的氢元素,所以若生成的氢气的质量相等,硫酸均反应完;故正确;
④.根据化学方程式![]() ,可知每56g铁生成2g氢气,根据化学方程式
,可知每56g铁生成2g氢气,根据化学方程式![]() ,可知每65g锌反应生成2g氢气;即可判断出生成等质量的氢气,消耗的金属质量不相等,故错误;
,可知每65g锌反应生成2g氢气;即可判断出生成等质量的氢气,消耗的金属质量不相等,故错误;
故答案为:![]() ;①③。
;①③。

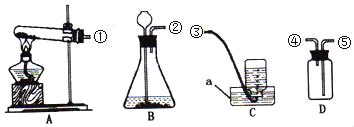
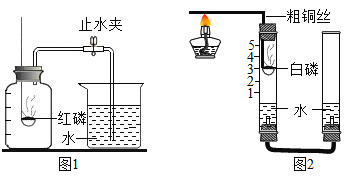
【题目】某科学兴趣小组的同学按照课本上的实验装置做“测定空气中氧气的体积分数”实验(如图1所示),但测出的氧气的体积分数明显小于![]() ,请你参与探究:
,请你参与探究:
(提出问题)
造成误差的原因是什么?如何改进课本上的实验装置?
(查阅资料)
1.红磷、白磷的一些性质如表:
颜色、状态 | 熔点/℃ | 着火点/℃ | 密度/(g/cm3) | |
红磷 | 暗红色固体 | 590 | 240 | 2.34 |
白磷 | 白色或黄色固体 | 44.1 | 40 | 1.82 |
2.铜能与氧气反应生成黑色的氧化铜。
(猜想与假没)
甲同学:可能是导管内原含有空气,后来留有吸入的水,影响实验的准确性。
乙同学:可能是瓶内残留气体中还有氧气。
你还能作出的猜想是_____。
(交流与讨论)
(1)丙同学认为用木炭代替红磷,就可以消除误差,你认为他的猜想_____(填“合理”或“不合理”)理由是_____。
(2)他们利用金属的导热性,对课本上的实验装置进行了图2所示的改进(其他仪器忽略)。
①甲同学提出应把红磷换为白磷,理由是_____。
②与课本上的实验装置相比较,该装置的一个优点是_____。
(探究与反思)
(1)为了验证乙同学的猜想,将铜粉放在残余气体中加热,观察到铜粉变黑色,证明乙同学的猜想_____(填“合理”或“不合理”)。
(2)大家用改进的实验装置(如图2所示)进行实验,待玻璃管冷却、管内白色的烟幕消失时,左玻璃管内的液面上升了1格,得到了较准确的结果。左玻璃管上端生成白色固体的有关化学方程式是:_____。
【题目】小李和小王同学对化学计算很有心得,以下是他们解答一道计算题的实录。请你一起参与研究并完成相关问题。( 计算结果精确到0.01g)
题目已知: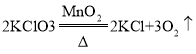 ,两位同学为了测定实验室中氯酸钾药品是否纯净,取2. 5g该药品与0. 5g二氧化锰混合。加热该混合物t3时间后(假设杂质不参加反应),冷却,称量剩余固体质量,重复以上操作,依次称得加t2 、t3、t4时间后剩余固体的质量,记录数据如下表:
,两位同学为了测定实验室中氯酸钾药品是否纯净,取2. 5g该药品与0. 5g二氧化锰混合。加热该混合物t3时间后(假设杂质不参加反应),冷却,称量剩余固体质量,重复以上操作,依次称得加t2 、t3、t4时间后剩余固体的质量,记录数据如下表:
加热时间 | t1 | t2 | t3 | t4 |
剩余固体质量/g | 2.12 | 2.08 | 2.04 | 2.04 |
(1)两同学一致认为氯酸钾已经完全反应的时间为_____(选填“t1”、 “t2”、“t3”、“t4”) 。
(2)小李根据质量守恒定律很快得到(2.5g+0.5g-2.04g)是_____(填化学式)的质量。
(3)请你计算:该药品中氯酸钾的质量,并判断该药品是否纯净?_____