题目内容
【题目】请仔细分析下列化学反应,回答下列问题:
①2H2+O2![]() 2H2O;②2CO+O2
2H2O;②2CO+O2![]() 2CO2;③ 3Fe+2O2
2CO2;③ 3Fe+2O2![]() Fe3O4
Fe3O4
(1)反应①~③有许多共同点。如:它们的生成物都属于____________。请你再指出它们的一个共同点:____________;
(2)反应①~③也有许多不同之处,请仿照示例指出其中一点(答案不能与示例相同)。示例:③的方程式中化学计量数之比为3︰2︰1,而另两个是2︰1︰2。不同之处:_______________。
【答案】氧化物 都是化合反应(其他合理答案也可) ②是化合物与O2反应,而另两个是单质与O2的反应(其他合理答案也可)
【解析】
(1)生成物都是由两种元素组成的,并且其中有一种元素为氧元素的化合物,属于氧化物;三个化学反应的相同点还有都是化合反应;都是氧化反应(都是与O2的反应);都放热;反应中都有元素化合价发生改变等等;故填:氧化物;都是化合反应(其他合理答案也可)。
(2)②是化合物与O2反应,而另两个是单质与O2的反应;(或:③生成的是金属氧化物,而另两个则是非金属氧化物;③的生成物中每个分子含7个原子,而另两个的则含3个;③是固体与O2的反应,而另两个则是气体与O2的反应;③的生成物是固体,而另两个的生成物不是固体;③的生成物为黑色,而另两个的生成物都是无色;②是有毒物质与O2的反应,而另两个是无毒物质与O2的反应;③是固体与氧气的反应,而另两个是气体与氧气的反应.③发生反应时没有火焰产生,而另两个有火焰产生)。故填:②是化合物与O2反应,而另两个是单质与O2的反应(其他合理答案也可)。

 A加金题 系列答案
A加金题 系列答案 全优测试卷系列答案
全优测试卷系列答案【题目】在饱和的碳酸钠溶液中通入CO2可用来制备碳酸氢钠(NaHCO3),发生反应的化学方程式为Na2CO3+CO2+H2O = 2NaHCO3。由于溶解度不同,饱和碳酸钠溶液中通入CO2会析出碳酸氢钠晶体而使溶液变浑浊。某化学课外小组同学发现不同条件下出现浑浊的时间不同。
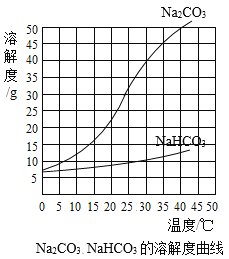
Na2CO3、NaHCO3的溶解度曲线
(提出问题)影响碳酸氢钠晶体产生速率的因素有哪些?
(猜想与假设)碳酸氢钠晶体产生速率的影响因素有温度、试管内径、CO2流速、饱和碳酸钠溶液的体积。
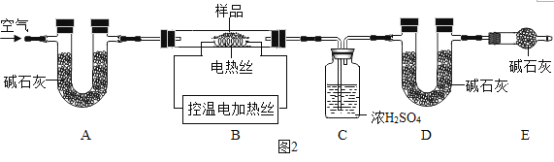
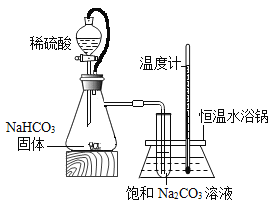
(进行实验)实验装置如下图所示。每次实验时均在试管里加入1mL饱和碳酸钠溶液并在试管后放置一张写有黑色字迹的白纸,从垂直于试管的方向观察白纸上字迹的清晰程度,记录时间,用于判断碳酸氢钠晶体的产生速率。部分实验记录如下表所示。
序号 | 温度 | 试管内径 | CO2流速 (个/秒) | 产生不同现象的时间 | ||
字迹变淡 | 字迹模糊 | 字迹消失 | ||||
① | 25 | 10 mm | 5-8 | 517" | 719" | 817" |
② | 32 | 10 mm | 5-8 | 350" | 409" | 428" |
③ | 40 | 10 mm | 5-8 | 348" | 406" | 418" |
④ | 25 | 14 mm | 5-8 | 636" | 738" | 828" |
⑤ | 25 | 25 mm | 5-8 | X | 943" | 1022" |
⑥ | 25 | 10 mm | 10-13 | 502" | 640" | 758" |
⑦ | 25 | 10 mm | 2-5 | 540" | 1045" | 1236" |
(解释与结论)
(1)由上述溶解度曲线图可获得的信息有________(写出一条即可)。
(2)锥形瓶中是利用碳酸氢钠与稀硫酸(H2SO4)反应来制二氧化碳。除生成二氧化碳外,还有水和硫酸钠(Na2SO4)生成,该反应的化学方程式为________。
(3)实验①④⑤研究的影响因素是________。
(4)表中X应该是________。
A 605" B 845" C 955"
(5)通过对数据的观察和分析,小明认为“二氧化碳流速越快,碳酸氢钠晶体产生速率越快”,得到该结论的依据是________(填实验序号)。
(6)结合实验①②③,可得出的结论是_________。
(7)若要研究饱和碳酸钠溶液的体积对碳酸氢钠晶体产生速率是否有影响,需要控制的变量有________。