题目内容
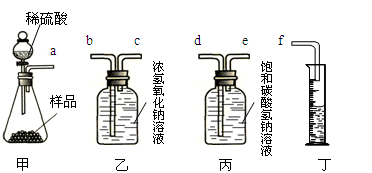
某化工厂生产的纯碱中含有少量的氯化钠。化学活动小组的同学合理利用下列装置对此样品进行分析。根据进入量筒中液体的体积来计算该样品中纯碱的含量。已知二氧化碳在饱和碳酸氢钠溶液中溶解度极小。
请你与活动小组的同学一起思考并回答下列问题:
(1)进行实验时,应选择上述装置中的 组合更合理(选填甲、乙、丙、丁)。所选装置各导管的连接顺序从左到右依次为 (填导管序号)。
(2)反应开始后,甲中有气泡产生,该反应的化学方程式为 。
(3)若甲中采用盐酸进行实验,测得数据与用稀硫酸时不一致,则采用稀盐酸时测得样品中纯碱的质量分数 (填较大、较小)。
(4)实验中,若样品取量过多,可能导致反应液体外溢,造成实验误差;若样品取量太少,会导致 ,也会造成实验误差。
(1)甲、丙、丁 a e d f
(2)Na2CO3 + H2SO4 = Na2SO4 + H2O + CO2↑
(3)较大
(4)生成的气体过少,气体压强太小,液体不能压入量筒中解析:
略
(2)Na2CO3 + H2SO4 = Na2SO4 + H2O + CO2↑
(3)较大
(4)生成的气体过少,气体压强太小,液体不能压入量筒中解析:
略

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
某化工厂生产的纯碱中含有少量NaCl杂质,其产品包装袋上标有:碳酸钠≥96%.为了证实该产品中碳酸钠的含量,某同学取12g该样品放入烧杯中,称得烧杯和样品总质量为132.0g再把100g稀盐酸平均分成4次加入烧杯中,每次充分反应后烧杯和剩余物总质量如下:(每次反应产生的CO2气体都全部从烧杯中逸出)
请你根据表中数据分析:①第1次充分反应后产生的CO2气体质量是______g
②该产品中碳酸钠的质量分数是多少?该产品是否合格?(计算后回答,计算结果精确到0.1%)
| 加入稀盐酸次数 | 1 | 2 | 3 | 4 |
| 加入稀盐酸质量/g | 25 | 25 | 25 | 25 |
| 充分反应后烧杯和剩余物总质量/g | 155.2 | 178.4 | 202.6 | 227.6 |
②该产品中碳酸钠的质量分数是多少?该产品是否合格?(计算后回答,计算结果精确到0.1%)