题目内容
【题目】下图是实验室制取气体的常用装置。
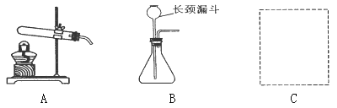
(1)写出一个用A装置制取O2的化学方程式:____________________。检验一瓶无色气体是O2的方法是___________________________,则证明该瓶中的气体为O2。
(2)制取CO2、O2、H2的发生装置都可选择B。试从反应物的状态、反应条件等方面总结满足B装置要求的一般条件有哪些?_________________
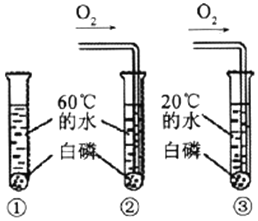
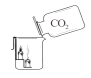
(3)请简述如图装置中实验现象产生的原因。_________________
(4)用试管采用排空气法收集H2 ,请在C处方框中画出装置图(只画试管和导气管)。____________
(5)称取10 g石灰石(杂质不参加反应),加入100 g稀盐酸,恰好完全反应,反应后剩余物质的总质量为106.7 g(气体的溶解忽略不计)。计算该样品中碳酸钙的质量分数。____________
【答案】2KMnO4 ![]() K2MnO4+MnO2+O2↑(或2KClO3
K2MnO4+MnO2+O2↑(或2KClO3 ![]() 2KCl+3O2↑ ) 将带火星的小木条伸入集气瓶中 反应物为固体(或液体)和液体、反应条件为常温 二氧化碳密度比空气大、不燃烧也不支持燃烧
2KCl+3O2↑ ) 将带火星的小木条伸入集气瓶中 反应物为固体(或液体)和液体、反应条件为常温 二氧化碳密度比空气大、不燃烧也不支持燃烧  75%
75%
【解析】
(1)A装置为固-固加热型,高锰酸钾法制取O2可以用装置A,化学方程式:2KMnO4 ![]() K2MnO4+MnO2+O2↑(氯酸钾法制氧气也可以用此装置,反应方程式为:2KClO3
K2MnO4+MnO2+O2↑(氯酸钾法制氧气也可以用此装置,反应方程式为:2KClO3 ![]() 2KCl+3O2↑)。氧气有助燃性,能使带火星的木条复燃,检验一瓶无色气体是O2的方法是将带火星的小木条伸入集气瓶中,木条复燃,则证明该瓶中的气体为O2;
2KCl+3O2↑)。氧气有助燃性,能使带火星的木条复燃,检验一瓶无色气体是O2的方法是将带火星的小木条伸入集气瓶中,木条复燃,则证明该瓶中的气体为O2;
(2)选择发生装置需要考虑的因素有:反应物的状态和反应条件(反应是否需要加热)制取CO2、O2、H2的发生装置都可选择B,是因为制取CO2、O2、H2的反应物为固体(或液体)和液体、反应条件为常温;
(3)向盛有高低两支蜡烛的烧杯用倒入二氧化碳,蜡烛由低到高逐渐熄灭,因为二氧化碳密度比空气大、不燃烧也不支持燃烧;
(4)用试管采用排空气法收集H2 ,应将试管口向下,将导管深入试管内,导管口接近试管底;
(5)设样品中碳酸钙的质量的质量为x
CO2的质量为:100 g+10 g-106.7 g=3.3 g

![]() =
=![]()
x=7.5 g
样品中碳酸钙的质量分数为:![]()
答:样品中碳酸钙的质量分数为75%