题目内容
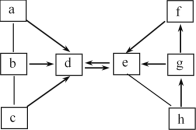
【题目】如图所示a—h是初中化学常见的物质,其中b,d是单质, f、g、h含有同种金属元素。图中“→”表示转化关系,“—”表示相互能反应。图中部分反应物、生成物已略去。以下说法正确的是
A. a可能是过氧化氢
B. a—h中只有一种氧化物
C. b→d,d→e的化学反应类型可能相同
D. 图中涉及到的化学反应只有一个是放热反应
【答案】C
【解析】
根据题给信息,e可以是H2O,f是CaCO3,g是Ca(OH)2,h是CaO,d是H2,c可以是稀H2SO4,a可以是稀HCl,b可以是Zn。A. a可能是稀硫酸或稀盐酸,此选项错误;
B. a—h中,e、h分别是H2O、CaO,都是氧化物,此选项错误;
C. b→d,d→e的化学反应分别是Zn+H2SO4==ZnSO4+H2↑、H2 +CuO![]() Cu+H2O,都是置换反应,反应类型相同,此选项正确;
Cu+H2O,都是置换反应,反应类型相同,此选项正确;
D. 图中涉及到的化学反应中Zn+H2SO4==ZnSO4+H2↑、CaO+H2O==Ca(OH)2都是放热反应,此选项错误。故选C。

【题目】请根据下列事实写出化学方程式。
(1)在氧气中燃烧火星四射的反应,生成黑色体固体_______。
(2)有两种氧化物参加的化合反应_______。
(3)酒精C2H5OH在空气中燃烧_______。
【题目】小雨阅读课外资料得知:氯酸钾的分解可用二氧化锰、氧化铜等物质作催化剂。于是,他对影响氯酸钾分解的因素及催化剂的催化效果产生了探究兴趣。
(提出问题)氧化铜是否比二氧化锰催化效果更好?影响氯酸钾分解速率的因素有哪些 呢?
(设计实验1小雨以生成等体积的氧气为标准,设计了下列几组实验。
序号 | KClO3的质量 | 其他物质的质量 | 温度 | 氧气的体积 | 反应所需时间 |
① | 10.0 g | 330℃ | 100 mL | t1 | |
② | 10.0 g | CuO 1.5 g | 330℃ | 100 mL | t2 |
③ | 10.0 g | MnO2 1.5 g | 330℃ | 100 mL | t3 |
④ | 10.0 g | MnO2 g | 380℃ | 100mL | t4 |
(1)若t1>t2,说明氧化铜能加快氯酸钾的分解速率。若要确定氧化铜是此反应的催化剂,还需探究反应前后,氧化铜的_________和_________不变。
(2)写出实验④所涉及的化学方程式__________________。
(3)实验④中MnO2的质量为_________g,若t3>t4,则化学反应快慢与温度的关系是_________。
(4)氯酸钾的分解速率可能还与_________因素有关,请设计实验证明_______。