题目内容
实验室有一瓶无色溶液,小明将无色的酚酞试液滴入溶液中变红色,以下说法正确的是( )
分析:根据已有的这是进行分析,酚酞在碱性溶液中为红色.
解答:解:A、显碱性的溶液不一定是碱的溶液,比如碳酸钠溶液呈碱性,碳酸钠属于盐类物质,故A错误;
B、酚酞试液在酸性溶液中为无色,故B错误;
C、溶液为酸性时,酚酞试液为无色,故C错误;
D、溶液为碱性时,酚酞为红色,故D正确;
故选D.
B、酚酞试液在酸性溶液中为无色,故B错误;
C、溶液为酸性时,酚酞试液为无色,故C错误;
D、溶液为碱性时,酚酞为红色,故D正确;
故选D.
点评:本题考查了指示剂的变色,完成此题,可以依据酚酞的性质进行.

练习册系列答案
相关题目
 (2010?崇左)实验室有一瓶无色溶液,由于腐蚀,其标签破损(如图).
(2010?崇左)实验室有一瓶无色溶液,由于腐蚀,其标签破损(如图).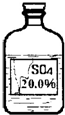 碱式碳酸铜[化学式为Cu2(OH)2CO3,相对分子质量为222]加热完全分解后得到的黑色固体是什么呢?甲、乙、丙三位同学想通过实验探究,来确定该黑色固体的组成.
碱式碳酸铜[化学式为Cu2(OH)2CO3,相对分子质量为222]加热完全分解后得到的黑色固体是什么呢?甲、乙、丙三位同学想通过实验探究,来确定该黑色固体的组成.