题目内容
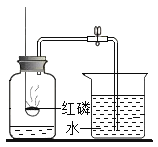
【题目】用镁条测定空气中氧气含量时(如图所示),实验完毕,冷却后进入左瓶的水的体积远大于总容积的1/5,且产生了淡黄色固体。某学习小组对此产生兴趣,进行了如下探究。

(资料)镁化合物的颜色:白色:MgO、Mg(OH)2、MgCl2、MgCO3、Mg(NO3)2;淡黄色:Mg3N2。
(猜想)淡黄色固体是Mg3N2,是由镁与氮气发生燃烧反应生成的。由于氮气和氧气都参与了反应,导致进入水的体积远大于总容积的1/5。
(实验)小组成员设计并进行了下列实验。

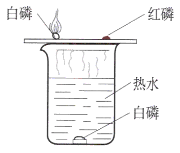
①将足量白磷在空气中点燃后,迅速伸入钟罩(钟罩下端无底)内,塞紧橡皮塞(图1);
②待钟罩内水面不再变化时,向水槽中加水,使水槽中液面与钟罩内液面相平;
③打开橡皮塞,将燃着的螺旋状镁条迅速伸入钟罩内,塞紧橡皮塞(图2)
④待钟罩内水面不再变化时,观察到钟罩内壁及表面皿中出现淡黄色固体。
(结论)小组同学的猜想正确。
(讨论)(1)镁在空气中燃烧的产物中一定不含氯化镁,理由是_____________________。
(2)步骤①中将足量白磷在钟罩内燃烧的目的是_____________________。
(3)通过以上探究,请写一点你对燃烧的新认识_____________________。
【答案】反应物中不含有氯元素 将氧气完全消耗,使实验结果更准确 燃烧不一定需要氧气参加
【解析】
(1)镁在空气中燃烧的产物中一定不含氯化镁,理由是反应物中不含有氯元素,因此不能生成氯化镁;
(2)步骤①中将足量白磷在钟罩内燃烧的目的是将氧气完全消耗,使实验结果更准确;
(3)通过以上探究可知,燃烧不一定需要氧气参加。

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目