题目内容
【题目】将含3克氯酸钾和1克二氧化锰的混合物加热片刻,冷却,称得残余固体的质量为3.04克,根据质量守恒定律可求:
(1)生成氧气的质量为多少克?
(2)固体残余物中含有什么物质?
(3)质量各为多少?
【答案】⑴0.96g;⑵二氧化锰、氯化钾、氯酸钾;⑶1g、1.49g、0.55g
【解析】(1)根据质量守恒定律,反应后固体减少的质量是生成氧气的质量:3g+1g-3.04g=0.96g。
(2)设生成0.96g氧气时,消耗氯酸钾的质量为x。
2KClO3 ![]() 2KCl+3O2↑
2KCl+3O2↑
245 96
x 0.96g
![]() =
=![]() ,解得x=2.45g,故氯酸钾没有完全反应,固体残余物中含有剩余的氯酸钾、作催化剂的二氧化锰、生成的氯化钾。
,解得x=2.45g,故氯酸钾没有完全反应,固体残余物中含有剩余的氯酸钾、作催化剂的二氧化锰、生成的氯化钾。
(3)设反应生成氯化钾的质量为y。
2KClO3 ![]() 2KCl+3O2↑
2KCl+3O2↑
149 96
y 0.96g
![]() =
=![]() ,解得y=1.49g
,解得y=1.49g
剩余氯酸钾的质量为:3g-2.45g=0.55g,二氧化锰在化学反应前后质量不变,还有1g的二氧化锰,故固体残余物中含有剩余的氯酸钾0.55g、作催化剂的二氧化锰1g、生成的氯化钾1.49g。

 仁爱英语同步练习册系列答案
仁爱英语同步练习册系列答案 学习实践园地系列答案
学习实践园地系列答案【题目】某化学兴趣小组同学在做铁与硫酸溶液反应的实验时,发现生成的气体有刺激性气味,于是进行了探究。
【提出问题】铁与硫酸溶液反应生成的气体为什么有刺激性气味?
【查阅资料】(1)6H2SO4(浓)+2Fe![]() Fe2(SO4)3+6 H2O +3SO2↑
Fe2(SO4)3+6 H2O +3SO2↑
(2)SO2可使酸性高锰酸钾溶液的紫红色褪去。
【进行猜想】铁与不同浓度的硫酸溶液反应,生成的气体产物中可能有二氧化硫。
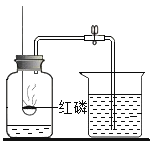
【实验探究】小明用图甲所示的装置进行实验,每次实验A中加入的硫酸溶液体积、铁粉的质量相同。D中收集到的气体进行如图乙所示的爆鸣实验。

请帮助化学兴趣小组同学完成下表:
A中硫 酸浓度 | 实验现象 | A中生成气体成分 | |||
B中酸性高锰酸钾溶液 | C中酸性高锰酸钾溶液 | 爆鸣实验 | |||
实验一 | 98% | __ | 不褪色 | __ | 只有SO2 |
实验二 | 50% | 稍有褪色 | 不褪色 | 有爆鸣声 | __ |
实验三 | 20% | ___ | 不褪色 | 有爆鸣声 | 只有H2 |
【实验结论】铁与不同浓度的硫酸溶液反应,生成的气体产物可能不同,当硫酸浓度达到足够大时,生成的气体产物中有二氧化硫。
【交流反思】写出实验二中发生爆鸣反应的化学方程式:_______。
写出实验三中铁与硫酸反应的化学方程式:_______。
【题目】学校研究性学习小组为了测定当地矿山石灰石中碳酸钙的质量分数,取来了一些矿石样品,并取稀盐酸200 g,平均分成4份进行实验,结果如下:
实验 | 一 | 二 | 三 | 四 |
加入样品的质量/g | 5 | 10 | 15 | 20 |
生成的CO2质量/g | 1.76 | 3.52 | 4.4 | m |
(1)上表中m的数值是 ;
(2)反应中矿石有剩余是第 次实验;
(3)这种石灰石矿中碳酸钙的质量分数是 ;
(4)稀盐酸中溶质的质量分数是 .