题目内容
某同学在测定空气里氧气含量时,待火焰熄灭后,立即打开止水夹,发现水沿导管进入集气瓶中,最终进入集气瓶的水的体积小于
,请你从以下几方面分析原因:
(1)药品方面:可能
(2)实验操作方面:
(3)装置方面:
| 1 | 5 |
(1)药品方面:可能
红磷的量不足
红磷的量不足
;也可能用燃烧的产物是气体的物质
燃烧的产物是气体的物质
作反应物进行了实验.(2)实验操作方面:
未等到装置冷却到室温就打开止水夹
未等到装置冷却到室温就打开止水夹
.(3)装置方面:
装置漏气
装置漏气
.分析:本题是测定空气中氧气的含量,我们常用燃烧红磷或白磷的方法,因为磷燃烧生成白色固体五氧化二磷,几乎不占空间,使得内外产生气压差,从而得到正确的结论.因此在选择可燃物时,必须考虑到:燃烧的条件;生成物的状态;不与空气中其他物质发生反应.保证本实验成功的关键是:①装置气密性好;②红磷要足量;③要冷却至室温再读数.
解答:解:实验完毕后,集气瓶中内水面上升明显小于瓶内空气体积的
,产生问题的原因可能是:
(1)药品方面:可能红磷的量不足,瓶内氧气没有消耗完;也可能用燃烧的产物是气体的物质作反应物进行了实验,装置内的压强变化不大.
(2)实验操作方面:未等到装置冷却到室温就打开止水夹,使进入瓶内的水的体积减少.
(3)装置方面:装置漏气,使进入瓶内的水的体积减少.
故答为:(1)红磷的量不足,燃烧的产物是气体的物质;(2)未等到装置冷却到室温就打开止水夹;(3)装置漏气.
| 1 |
| 5 |
(1)药品方面:可能红磷的量不足,瓶内氧气没有消耗完;也可能用燃烧的产物是气体的物质作反应物进行了实验,装置内的压强变化不大.
(2)实验操作方面:未等到装置冷却到室温就打开止水夹,使进入瓶内的水的体积减少.
(3)装置方面:装置漏气,使进入瓶内的水的体积减少.
故答为:(1)红磷的量不足,燃烧的产物是气体的物质;(2)未等到装置冷却到室温就打开止水夹;(3)装置漏气.
点评:考点考查了空气中氧气的含量的探究,并且注重了实验方案的评价,对实验方案进行评价是近几年中考的一个重点.评价包括对实验方案的评价、实验过程的评价、实验结论的评价等,要认真把握.

练习册系列答案
相关题目



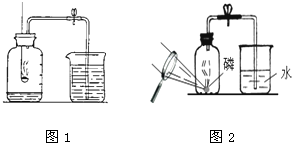 如图1是“测定空气里氧气含量”实验的装置.
如图1是“测定空气里氧气含量”实验的装置.