题目内容
【题目】质量守恒定律的发现,对化学的发展做出了重要贡献。

(1)通过分别称量下列两组试剂在密闭容器内混合前后的总质量,能验证质量守恒定律的是____(填标号)。
a大理石和稀盐酸 bNaOH溶液和Na2SO4溶液
(2)在足量氧气中点燃镁条的实验过程中,固体质最变化如图一。
①从燃烧条件分析,固体质量在t1前没有发生变化的原因是___________。
②该反应的化学方程式为__________。
③参加反应的氧气质量为__________g。
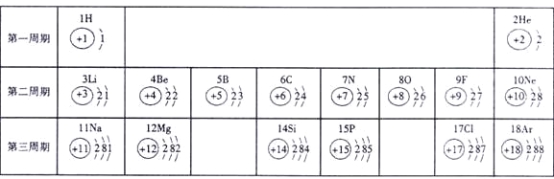
(3)在一定条件下,A和B反应生成C,微观示意图如图二。回答下列问题:
①一个A分子由____个原子构成。
②C分子中元素的质量比N:O=____。
③上述反应中一定发生改变的是___________(填标号)。
a元素种类b原子种类c分子种类
【答案】a 温度未达到金属的着火点 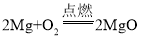 1.6 2 7:16 c
1.6 2 7:16 c
【解析】
(1)大理石和稀盐酸反应生成氯化钙、二氧化碳和水,反应前后的质量一样,能够验证质量守恒定律,a正确,而NaOH溶液和Na2SO4溶液不能发生反应,无法验证。故选a;
(2)①固体质量在t1前没有发生变化的原因是因为温度未达到金属的着火点,反应尚未开始;
②镁条在氧气中燃烧生成氧化镁,反应的化学方程式为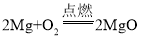 ;
;
③由图一可以看出,反应前镁条的质量为2.4g,反应后氧化镁的质量为4g,由质量守恒定律可知,参与反应的氧气的质量为4g-2.4g=1.6g;
(3)①由图二可以看出一个A分子由2个原子构成;
②C分子中含有一个N原子,2个O原子,元素的质量比N:O=14:32=7:16;
③由质量守恒定律可知,反应前后元素种类和原子种类都不会发生变化,一定会发生变化的是分子种类,故选c。

【题目】实验室现有氯化镁和硫酸钠的固体混合物样品,小明同学想测定样品中氯化镁的质量分数。先称取该混合物样品20g,完全溶于水中。然后取用了一定溶质质量分数的氢氧化钠溶液100g平均分四次加入其中,充分振荡,实验所得数据见下表,请你分析并进行有关计算:
| 1 | 2 | 3 | 4 |
加入氢氧化钠溶液的质量/g | 25 | 25 | 25 | 25 |
生成沉淀的质量/g | 2.9 | x | 8.7 | 8.7 |
(1)上表中x的数值为____________;
(2)计算原固体混合物样品中氯化镁的质量分数是多少_______?