题目内容
【题目】(1)用化学用语表示:
①2个氮分子______________②3个硫酸根离子___________
③碳酸钠_________________④氦气________
⑤保持二氧化碳化学性质的最小微粒___________
(2)写出下列符号的意义
①![]() _______________②
_______________②![]() _________________
_________________
(3)配平下列化学方程式
①____CO+____Fe3O4![]() ___Fe+____CO2
___Fe+____CO2
②___C2H5OH+____O2![]() ______CO2+_____H2O
______CO2+_____H2O
③___Al+____HCl=____AlCl3+_____H2![]()
【答案】2N2 3SO42- Na2 CO3 He CO2 4个亚铁离子 五氧化二磷中磷元素的化合价为+5 4 1 3 4 1 3 2 3 2 6 2 3
【解析】
(1)①2个氮分子就是在氮气化学式的前面加上数字2,表示为:2N2 ;
②3个硫酸根离子就是在硫酸根离子的前面加上数字3,表示为:3SO42- ;
③碳酸钠中钠元素为+1价,碳酸根为-2价,其化学式为Na2 CO3 ;
④氦气是由原子直接构成的物质,因此其化学式可以直接由元素符号表示,表示为:He;
⑤保持二氧化碳化学性质的最小微粒是二氧化碳分子,表示为:CO2 。
(2)①![]() 表示4个亚铁离子;
表示4个亚铁离子;
②![]() 表示五氧化二磷中磷元素的化合价为+5;
表示五氧化二磷中磷元素的化合价为+5;
(3) ①本题可从得失氧的角度配平,一个CO分子反应中获得一个氧原子生成一个CO2分子,由于一个Fe3O4分子中氧原子的数目为4个,若Fe3O4前的化学计量数为1,则CO与CO2 前面的化学计量数都为4,根据铁元素守恒, Fe前面的化学计量数分别3。故配平后的反应方程式为:4CO+Fe3O4![]() 3Fe+4 CO2,化学计量数分别为:4、1、3、4。
3Fe+4 CO2,化学计量数分别为:4、1、3、4。
②本题可利用“定一法”进行配平,把C2H5OH的化学计量数定为1,根据碳、氢元素守恒,CO2、H2O的化学计量数分别为2、3,根据氧元素守恒,O2的化学计量数为3,故配平后的化学方程式为:C2H5OH+3O2![]() 2CO2+3H2O,化学计量数分别为:1、3、2、3。
2CO2+3H2O,化学计量数分别为:1、3、2、3。
③本题可利用“定一法”进行配平,把AlCl3 的化学计量数定为1,则Al、HCl、H2的化学计量数分别为:1、3、![]() ,同时扩大2倍,则配平后的化学方程式为:2Al+6HCl=2AlCl3+3H2
,同时扩大2倍,则配平后的化学方程式为:2Al+6HCl=2AlCl3+3H2![]() ,化学计量数分别为:2、6、2、3。
,化学计量数分别为:2、6、2、3。

【题目】KNO3和KCl在不同温度时的溶解度如下表所示,请回答下列问题:
温度/℃ | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 70 | |
溶解度/g | KNO3 | 13.3 | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | 110 | 138 |
KCl | 27.6 | 31.0 | 34.6 | 37 | 40.0 | 42.6 | 45.5 | 48.3 | |
(1)依据上表数据,已经绘出KNO3和KCl的溶解度曲线如图,图中能表示KNO3溶解度曲线的是____________。(填“m”或“n”)

(2)10℃时,131g饱和KCl溶液,蒸发10g水后,再降温到10℃,可析出KCl晶体的质量为___________g。
(3)根据溶解度曲线可以知道,若从m的饱和溶液中析出晶体,应采用______________的方法。
(4)溶液A时70℃含有120g水的KNO3溶液,经过如下操作,得到102g KNO3固体。
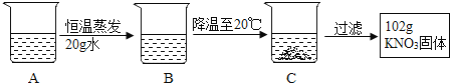
Ⅰ.B溶液为__________(选填“饱和”或“不饱和”)溶液
Ⅱ.对以上过程的分析,正确的是____________(选填编号)
a.A到B的过程中,溶质质量没有改变 b.B中溶质与溶剂的质量比为138:100
c.A溶液一定是不饱和溶液 d.A溶液的质量等于222g