题目内容
【题目】KNO3和KCl在不同温度时的溶解度如下表所示,请回答下列问题:
温度/℃ | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 70 | |
溶解度/g | KNO3 | 13.3 | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | 110 | 138 |
KCl | 27.6 | 31.0 | 34.6 | 37 | 40.0 | 42.6 | 45.5 | 48.3 | |
(1)依据上表数据,已经绘出KNO3和KCl的溶解度曲线如图,图中能表示KNO3溶解度曲线的是____________。(填“m”或“n”)

(2)10℃时,131g饱和KCl溶液,蒸发10g水后,再降温到10℃,可析出KCl晶体的质量为___________g。
(3)根据溶解度曲线可以知道,若从m的饱和溶液中析出晶体,应采用______________的方法。
(4)溶液A时70℃含有120g水的KNO3溶液,经过如下操作,得到102g KNO3固体。
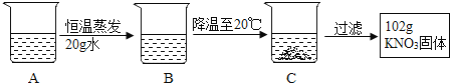
Ⅰ.B溶液为__________(选填“饱和”或“不饱和”)溶液
Ⅱ.对以上过程的分析,正确的是____________(选填编号)
a.A到B的过程中,溶质质量没有改变 b.B中溶质与溶剂的质量比为138:100
c.A溶液一定是不饱和溶液 d.A溶液的质量等于222g
【答案】m 3.1 降温结晶 不饱和 ac
【解析】
(1)依据上表数据可知,KNO3溶解度受温度影响较大,KCl溶解度受温度影响较小,根据溶解度曲线可知,图中m溶解度受温度影响较大,n溶解度受温度影响较小,所以图中能表示KNO3溶解度曲线的是m;
(2)根据题意和溶解度的涵义可知,10℃时,10g水与析出的晶体恰好能形成饱和溶液。设:可析出KCl晶体的质量为x,则有:![]() ,x=3.1g;
,x=3.1g;
(3)根据溶解度曲线可以知道,m溶解度随温度的降低而减小,且受温度影响较大,若从m的饱和溶液中析出晶体,应采用降温结晶的方法;
(4)Ⅰ、根据题意可知,B溶液温度是70℃,溶液中水的质量为100g,KNO3的质量为102g,70℃时,KNO3溶解度为138g,根据溶解度涵义可知,70℃时100g 水与138 g KNO3 恰好形成饱和溶液,所以B溶液为不饱和溶液;
Ⅱ、 a、根据Ⅰ中分析可知,B溶液为不饱和溶液,A到B的过程中,溶质质量没有改变,故a正确;
b、B溶液温度是70℃,溶液中水的质量为100g,KNO3的质量为102g,B中溶质与溶剂的质量比=102:100,故b错误;
c、70℃时,KNO3溶解度为138g,根据溶解度涵义可知,70℃时100g 水与138 g KNO3 恰好形成饱和溶液,A溶液中水的质量为120g, KNO3的质量为102g,A溶液一定是不饱和溶液,故c正确。故选ac。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】向100g水中不断加入固体A或改变温度,得到相应的溶液①~⑤。下列说法正确的是( )
![]()
资料:A的溶解度 | |||||
温度/℃ | 20 | 30 | 40 | 50 | 60 |
溶解度/g | 37.2 | 41.4 | 45.8 | 50.4 | 55.2 |
A. ②中A的质量分数最大 B. ③⑤中A的质量分数相等
C. ②④⑤的溶液为饱和溶液 D. ①③④⑤中没有固体存在