题目内容
【题目】工业上从海水中提取出含MgCl2、KCl两种物质的混合物,为了测定其中KCl的质量分数,现进行如下测定:取混合样品10.0g,向其中加入100g水,完全溶解后,分5次滴加KOH溶液,生成沉淀的质量与加入KOH溶液的质量关系如下表所示。
次数 | 第1次 | 第2次 | 第3次 | 第4次 | 第5次 |
滴加KOH溶液的质量/g | 10 | 10 | 10 | 10 | 10 |
产生沉淀的质量/g | 0.725 | 1.450 | 2.175 | 2.900 | 2.900 |
(1)通过表格可知,第 次滴加KOH溶液刚好完全反应。
(2)求反应后最终得到的混合溶液中KCl的质量分数。(计算结果精确到0.01%)
(3)请在坐标图中画出沉淀质量和加入KOH溶液质量的关系图。
(4)若用一定浓度的AgNO3溶液代替KOH,通过消耗硝酸银溶液质量来测定KCl的质量分数,测定值将会 (选填“偏大”“偏小”或“无影响”)。
【答案】
【1】
【2】 (1)4;(2)8.08%;(3);(4)偏大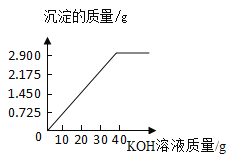
【解析】
(1)由表中的数据可知,每加入10g的氢氧化钾溶液产生沉淀的质量是0.725g,第四次加入时生成了沉淀是2.900g,再加入氢氧化钾不再生成沉淀,说明了第4次滴加KOH溶液刚好完全反应;
(2)设氯化镁的质量为x,生成的氯化钾的质量为y

![]()
![]()
解得:x=4.750g y=7.45g
反应后最终得到的混合溶液中KCl的质量分数:![]() ≈8.08%
≈8.08%
答:反应后最终得到的混合溶液中KCl的质量分数为8.08%。
(3)由上述计算可知,加入40g的氢氧化钾溶液时恰好完全反应生成沉淀的质量为2.900g,作出图示如下:
(4)由于氯化镁、氯化钾都能与硝酸银反应生成氯化银沉淀,由消耗硝酸银溶液质量来测定KCl的质量分数,测定值将会偏大。

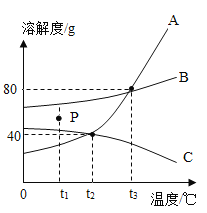
【题目】下列各选项与如图所示曲线相符的是
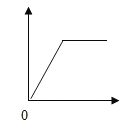
选项 | 横坐标 | 纵坐标 |
A | 向一定量的稀盐酸中加入锌粉的质量 | 溶液中氢元素的质量 |
B | 一定量的高锰酸钾固体受热 | 固体中锰元素的质量 |
C | 向一定量的澄清石灰水中加入碳酸钠溶液的质量 | 生成沉淀的质量 |
D | 在一定温度下,向一定量的饱和氯化钠溶液中加入硝酸钾固体的质量 | 溶液中总溶质的质量分数 |
A.AB.BC.CD.D
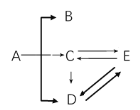
【题目】某化学课堂围绕“酸碱中和反应”,将学生分成若干小组开展探究活动。请你和他们一起完成以下实验探究。
【演示实验】将一定量稀盐酸加入到盛氢氧化钙溶液的小烧杯中。该反应的化学方程式是_____________。
【查阅资料】CaC12 滚液显中性
【提出问题】实验中未观察到明显现象,部分同学产生了疑问:反应后溶液中溶质的成分是什么?
【猜想与假设】针对疑问,甲组同学猜想如下:
猜想I:只有CaC12 猜想II:有__________
猜想III:有CaC12和Ca(OH)2 猜想IV:有CaCl2、HCl和Ca(OH)2
乙组同学对以上猜想提出质疑,认为猜想IV不合理,其理由是_________________。
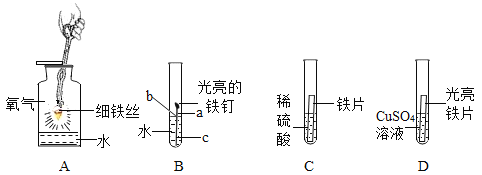
【实验探究】为了验证其余猜想,各小组进行了下列三个方案的探究。
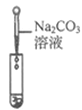
实验方案 | 滴加紫色石蕊溶液 | 通入CO2 | 滴加Na2CO3溶液 |
实验操作 |
|
|
|
实验现象 | ____________ | __________ | 产生白色沉淀 |
实验结论 | 溶液中含有Ca(OH)2 | 溶液中含有Ca(OH)2 | 溶液中含有Ca(OH)2 |
【得出结论】通过探究,全班同学一致确定猜想III是正确的。
【评价反思】(1)丙组同学认为滴加Na2CO3溶液产生白色沉淀,并不能证明溶液中一定含有Ca(OH)2,请你帮助他们说明原因____________。
(2)在分析反应后所得溶液中溶质的成分时,除了考虑生成物外.还需要考虑_______。