题目内容
【题目】在天平(灵敏度极高)两边的烧杯中分别盛有同质量、同溶质质量分数的稀硫酸,天平平衡,再向两烧杯中分别加入相同质量的镁和铁,充分反应后,若天平平衡,则反应物中一定有剩余的物质是_____________,一定没有剩余的物质是_______________;若天平失去平衡,则一定没有剩余的物质是______________________.
【答案】Mg或镁 稀硫酸 Fe或铁
【解析】
若天平平衡,说明生成的氢气质量相等,氢气是金属从稀硫酸中置换出来的氢组成的,故消耗的硫酸质量相等且没有剩余;
根据等质量金属完全反应放出氢气质量= ![]() ,因为镁原子的相对质量<铁原子的相对原子质量,所以如果生成氢气的质量相等,则反应的铁的质量应该大于镁的质量,故一定有剩余的是镁(Mg),可能有剩余的是铁,一定没有剩余的是稀硫酸。
,因为镁原子的相对质量<铁原子的相对原子质量,所以如果生成氢气的质量相等,则反应的铁的质量应该大于镁的质量,故一定有剩余的是镁(Mg),可能有剩余的是铁,一定没有剩余的是稀硫酸。
“加入质量相等的镁和铁”,若天平失去平衡,因为![]() ﹤
﹤![]() ,所以一定是镁产生的氢气多,则指针一定偏向放入金属铁的一方,铁(Fe)一定没有剩余。
,所以一定是镁产生的氢气多,则指针一定偏向放入金属铁的一方,铁(Fe)一定没有剩余。

 名校课堂系列答案
名校课堂系列答案【题目】工业上从海水中提取出含MgCl2、KCl两种物质的混合物,为了测定其中KCl的质量分数,现进行如下测定:取混合样品10.0g,向其中加入100g水,完全溶解后,分5次滴加KOH溶液,生成沉淀的质量与加入KOH溶液的质量关系如下表所示。
次数 | 第1次 | 第2次 | 第3次 | 第4次 | 第5次 |
滴加KOH溶液的质量/g | 10 | 10 | 10 | 10 | 10 |
产生沉淀的质量/g | 0.725 | 1.450 | 2.175 | 2.900 | 2.900 |
(1)通过表格可知,第 次滴加KOH溶液刚好完全反应。
(2)求反应后最终得到的混合溶液中KCl的质量分数。(计算结果精确到0.01%)
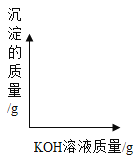
(3)请在坐标图中画出沉淀质量和加入KOH溶液质量的关系图。
(4)若用一定浓度的AgNO3溶液代替KOH,通过消耗硝酸银溶液质量来测定KCl的质量分数,测定值将会 (选填“偏大”“偏小”或“无影响”)。