题目内容
【题目】元素周期表是学习和研究化学的重要工具。溴元素的相关信息如图一所示,回答下列问题:
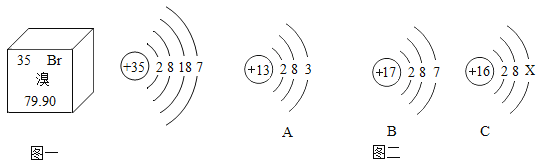
(l)溴元素的化学性质与图二哪种元素的化学性质相似_______(填元素符号)。
(2)溴元素与图二中A元素形成化合物的化学式为:_______。
(3)若图二中C表示离子,则离子符号是_______。
【答案】Cl AlBr3 S2-
【解析】
(1)决定元素化学性质的是最外层电子数,原子的最外层电子数相同,具有相似的化学性质;由题干中提供的结构示意图可知,溴原子的最外层电子数为7,则与其化学性质相似的粒子结构示意图中最外层电子数也应为7,图二中的B符合要求,其元素符号为Cl。
(2)A元素为铝元素,化合价为+3价;溴原子的最外层电子数为7,在化学反应中易得到1个电子而形成1个单位负电荷的阴离子,化合价的数值等于离子所带电荷的数值,且符号一致,则该元素的化合价为-1价;铝元素显+3价,溴元素显-1价,组成化合物的化学式为AlBr3。
(3)图二中C表示离子,则其最外层电子数为8,质子数=16,核外电子数=18,质子数<核外电子数,为硫离子,其离子符号为:S2-。

 亮点激活精编提优100分大试卷系列答案
亮点激活精编提优100分大试卷系列答案【题目】为了鉴别碳酸钠溶液和氢氧化钠溶液,同学们进行了探究实验。分别取两种溶液于两支试管中,各滴入一定量的氯化钙溶液,观察到其中一支试管中出现白色浑浊。实验结束后,同学们将废液倒入同一个干净的烧杯中,发现废液变浑浊,同学们对废液进行了过滤,并对滤液的成分进行了探究。
[提出问题]滤液中除水外还含有哪些物质?
[猜想]A可能含有氢氧化钠、氯化钠和氯化钙;
B可能含有氢氧化钠、氯化钠、碳酸钠和氯化钙;
C可能含有氢氧化钠、氯化钠。
你认为还可能是含有_______(写出一种猜想)。
[讨论]你认为猜想________(填字母代号)不合理,请说明理由______(用化学方程式表示)。
[实验设计]设计一个简单的实验,证明你的猜想正确。
实验步骤 | 实验现象 | 实验结论 |
取少许滤液于试管中,向试管中滴加_______ | _______ | 猜想正确 |
[反思交流]在分析化学反应后所得物质的成分时,除考虑生成物外,还需考虑反应物是否过量。
【题目】工业上从海水中提取出含MgCl2、KCl两种物质的混合物,为了测定其中KCl的质量分数,现进行如下测定:取混合样品10.0g,向其中加入100g水,完全溶解后,分5次滴加KOH溶液,生成沉淀的质量与加入KOH溶液的质量关系如下表所示。
次数 | 第1次 | 第2次 | 第3次 | 第4次 | 第5次 |
滴加KOH溶液的质量/g | 10 | 10 | 10 | 10 | 10 |
产生沉淀的质量/g | 0.725 | 1.450 | 2.175 | 2.900 | 2.900 |
(1)通过表格可知,第 次滴加KOH溶液刚好完全反应。
(2)求反应后最终得到的混合溶液中KCl的质量分数。(计算结果精确到0.01%)
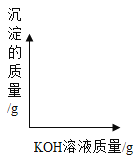
(3)请在坐标图中画出沉淀质量和加入KOH溶液质量的关系图。
(4)若用一定浓度的AgNO3溶液代替KOH,通过消耗硝酸银溶液质量来测定KCl的质量分数,测定值将会 (选填“偏大”“偏小”或“无影响”)。