题目内容
【题目】高纯氧化锌(ZnO)可作为紫外线吸收剂应用于化妆品中,其一种生产工艺如下
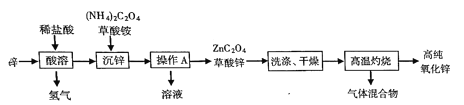
(1)推测草酸的化学式是______________。
(2)“沉锌”过程中发生复分解反应,反应的化学方程式为__________________。
(3)“操作A"的名称是___________________。
(4)检验草酸锌已洗净的方法是:取最后一次洗涤液少许于试管中,滴加____________,若无沉淀产生,则已洗净。
(5)“高温灼烧”时草酸锌分解生成三种氧化物,反应的化学方程式为__________
【答案】H2C2O4 ZnCl2+(NH4)2C2O4=ZnC2O4![]() +2NH4CI 过滤 AgNO3溶液 ZnC2O4
+2NH4CI 过滤 AgNO3溶液 ZnC2O4![]() ZnO+CO↑+CO2↑
ZnO+CO↑+CO2↑
【解析】
(1)草酸根显-2价,据此推测草酸的化学式是H2C2O4。故填:H2C2O4
(2)“沉锌”过程中发生复分解反应,反应的化学方程式是:ZnCl2+(NH4)2C2O4=ZnC2O4![]() +2NH4CI。故填:ZnCl2+(NH4)2C2O4=ZnC2O4
+2NH4CI。故填:ZnCl2+(NH4)2C2O4=ZnC2O4![]() +2NH4CI
+2NH4CI
(3)“操作A”是将液体与难溶性固体分离,是过滤;故填:过滤
(4)草酸锌是否已洗净,取最后一次洗涤液少许于试管中,看里面还有没有氯化铵,可以通过检验氯离子来检验,检验氯离子一般采用AgNO3溶液,若无沉淀产生,则已洗净。故填:AgNO3溶液
(5)“高温灼烧”时草酸锌分解得气体混合物,可推知气体为一氧化碳和二氧化碳,反应的化学方程式是:ZnC2O4![]() ZnO+CO↑+CO2↑;故填:ZnC2O4
ZnO+CO↑+CO2↑;故填:ZnC2O4![]() ZnO+CO↑+CO2↑
ZnO+CO↑+CO2↑

 芝麻开花课程新体验系列答案
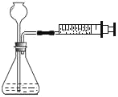
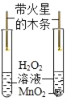
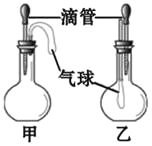
芝麻开花课程新体验系列答案【题目】如图所示的甲、乙两个装置中,胶头滴管中吸入某种液体,平底烧瓶中充入(或放入)另一种物质,挤压胶头滴管加入液体,一段时间后两装置中的气球都明显胀大(忽略液体体积对气球体积的影响)。则滴管和烧瓶中所用试剂可能是( )
甲 | 乙 | |
A. | 稀硫酸和铜片 | 水和硝酸铵固体 |
B. | 水和氢氧化钠固体 | AgNO3溶液和稀盐酸 |
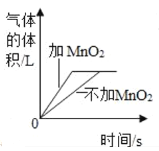
C. | 双氧水和MnO2 | NaOH溶液和CO2 |
D. | Na2CO3溶液和稀硫酸 | 水和浓硫酸 |
A. AB. BC. CD. D