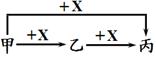题目内容
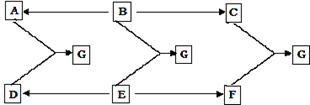
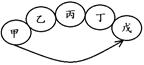
甲、乙、丙、丁、戊是初中化学常见的物质。下图中的五个圆分别表示这五种物质,用两圆相切表示这两种物质能发生反应,“→”表示物质间的转化关系(部分反应物、生成物及反应条件已略去)。
(1)若单质甲粉末与化合物戊均为黑色固体,丙和无色气体丁反应可以生成甲。戊的化学式是 ,乙和丙反应的化学方程式是 。
(2)若甲是铜绿的主要成分碱式碳酸铜【化学式为Cu2(OH)2CO3】,甲与酸反应生成一种盐及两种氧化物丁和戊,乙是胃酸的主要成分,乙与丙、丙与丁反应均可生成戊且无明显现象。甲和乙反应的化学方程式是 ,丙和丁反应的化学方程式是 。
(3)若五种物质所含元素为H、C、O、Na、Ca、S中的两种或三种,甲与丙属于同一类
物质,且相对分子质量由甲到戊依次增大。丙的俗称是 ,甲和丁反应的化学方
程式是 。

(1)若单质甲粉末与化合物戊均为黑色固体,丙和无色气体丁反应可以生成甲。戊的化学式是 ,乙和丙反应的化学方程式是 。
(2)若甲是铜绿的主要成分碱式碳酸铜【化学式为Cu2(OH)2CO3】,甲与酸反应生成一种盐及两种氧化物丁和戊,乙是胃酸的主要成分,乙与丙、丙与丁反应均可生成戊且无明显现象。甲和乙反应的化学方程式是 ,丙和丁反应的化学方程式是 。
(3)若五种物质所含元素为H、C、O、Na、Ca、S中的两种或三种,甲与丙属于同一类
物质,且相对分子质量由甲到戊依次增大。丙的俗称是 ,甲和丁反应的化学方
程式是 。
(1) Fe3O4 Fe2O3+ 3H2SO4 = Fe2(SO4)3+ 3H2O(写氧化铁与盐酸反应等可得分)
(2)Cu2(OH)2CO3+ 4HCl=2CuCl2 +CO2↑+3H2O 2NaOH + CO2=Na2CO3+H2O
(3)熟石灰或消石灰 2NaOH+ H2SO4=Na2SO4+2H2O
(2)Cu2(OH)2CO3+ 4HCl=2CuCl2 +CO2↑+3H2O 2NaOH + CO2=Na2CO3+H2O
(3)熟石灰或消石灰 2NaOH+ H2SO4=Na2SO4+2H2O
试题分析:(1)若单质甲粉末与化合物戊均为黑色固体,丙和无色气体丁反应可以生成甲。则甲是铁,乙是酸,硫酸或者盐酸均可,丙是氧化铁,丁是氢气,戊是四氧化三铁,戊的化学式是Fe3O4,乙和丙反应的化学方程式是Fe2O3+ 3H2SO4 = Fe2(SO4)3+ 3H2O,或者Fe2O3+ 6HCl = 2FeCl3+ 3H2O。
(2)若甲碱式碳酸铜【化学式为Cu2(OH)2CO3】,甲与酸反应生成一种盐,即氯化铜,及两种氧化物丁和戊,即水和二氧化碳,乙是胃酸的主要成分,即盐酸,乙与丙、丙与丁反应均可生成戊且无明显现象,则丙是氢氧化钠,丁是二氧化碳。甲和乙反应的化学方程式是Cu2(OH)2CO3+ 4HCl=2CuCl2 +CO2↑+3H2O,丙和丁反应的化学方程式是2NaOH + CO2=Na2CO3+H2O。
H、C、O、Na、Ca、S中的两种或三种可组成的常见物质有:水、二氧化碳、一氧化碳、二氧化硫、氧化钠、氧化钙、甲烷、氢氧化钠、氢氧化钙、碳酸、硫酸、碳酸钠、碳酸钙等。一氧化碳和甲烷与其它物质不反应,碳酸不稳定,可排除。两圆相切表示这两种物质能发生反应,甲与丙属于同一类物质,且相对分子质量由甲到戊依次增加,甲若为水或者其它氧化物,则丙为二氧化碳、二氧化硫、氧化钠、氧化钙中的一种,不符合两圆相切表示这两种物质能发生反应的已知条件,而相对分子质量由甲到戊依次增加,所以甲应为氢氧化钠,丙为氢氧化钙,氢氧化钙俗名熟石灰或消石灰;按相对分子质量,乙为二氧化硫或二氧化碳,丁为硫酸,戊为盐,且能与硫酸反应,只能是碳酸盐,为碳酸钠、碳酸钙;所以甲和丁反应的化学方程式是2NaOH+H2SO4=Na2SO4+2H2O。
点评:本题难度较大,根据题意,展开合理的联想,再带入题目进行验证,是解答推断题的常用方法。
书写化学方程式要遵循客观事实和质量守恒定律两个原则,注意化学式要正确,不要忘记反应条件、气体或者沉淀符号。

练习册系列答案
相关题目