题目内容
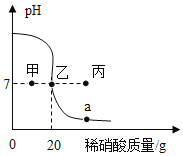
【题目】常温下,一锥形瓶中盛有20g溶质质量分数为4%的氢氧化钠溶液,先向其中滴加2滴酚酞试液,再逐滴滴加溶质质量分数为6.3%的稀硝酸,用pH传感器测得溶液的pH与加入稀硝酸的关系曲线如图。请回答问题:
(1)本实验反应的化学方程式是____。
(2)pH=7时,锥形瓶中的溶液呈____色,此时溶液的溶质质量分数是____(结果精确到0.01%)。
(3)图中a点对应的溶液中溶质的化学式是____。
(4)若改用溶质质量分数为12.6%的稀硝酸进行本实验,pH传感器测得的曲线可能经过____(填“甲”“乙”或“丙”)点。
【答案】NaOH+HNO3=NaNO3+H2O 无 4.25% HNO3、NaNO3 甲
【解析】
(1)氢氧化钠和稀硝酸反应生成硝酸钠和水,反应的化学方程式是:NaOH+HNO3=NaNO3+H2O;
(2)pH=7时,锥形瓶中的溶液显中性,呈无色;设反应生成硝酸钠质量为x,

![]()
x=1.7g,此时溶液的溶质质量分数是:![]() ;
;
(3)图中a点对应的溶液中溶质过量的硝酸和反应生成的硝酸钠,化学式是HNO3、NaNO3;
(4)若改用溶质质量分数为12.6%的稀硝酸进行本实验,恰好完全反应时需要硝酸质量减小,pH传感器测得的曲线可能经过甲点。

【题目】类价二维图反映的是元素的化合价与物质类别之间的关系,构建类价二维图是化学学习的重要方法。图1是某同学绘制的关于碳元素的类价二维图。
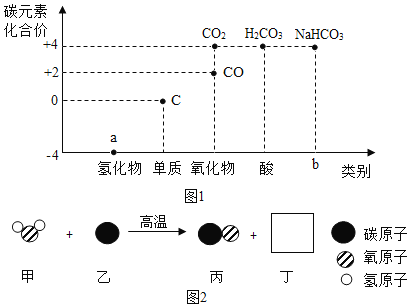
(1)a处氢化物为天然气的主要成分,其化学式为_______:b处对应物质的类别是_______。
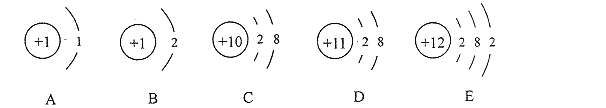
(2)煤的主要成分是单质碳。图2是用煤合成水煤气的反应微观示意图。该反应中方框丁中微粒的图示为_______,甲对应的物质表现出了_______性。
(3)类价二维图中的物质在一定条件下可以相互转化。请从含碳物质中选择合适物质完成下列表格:
转化类型 | 转化的化学方程式 | 反应用途 |
碳元素化合价升高 | _______ | 工业炼铁 |
碳元素化合价不变 | NaHCO3+HCl=NaCl+CO2↑+H2O | _______ |