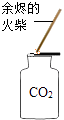题目内容
【题目】请结合下列实验装置图回答有关问题. 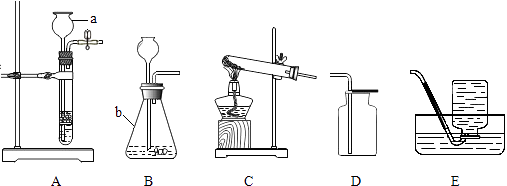
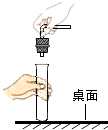
(1)仪器:a用途 , b名称 .
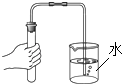
(2)实验室制取二氧化碳气体,装置A、B都可用作发生装置,其中可以控制反应进行的是(填装置序号),反应的化学方程式是 .
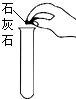
(3)同学们分析认为③中剩余溶液中一定有氯化钙,可能有盐酸.为验证是否含有盐酸,他们采用不同方案进行实验,得出相同的结论.
实验操作 | 实验现象 | 结论 | |
方案一 | 取样,加一枚生锈的铁钉 | 有盐酸 | |
方案二 | 取样,滴加AgNO3溶液和稀硝酸 | 产生白色沉淀 |
上述实验方案中,合理的是(选填:“方案一”或“方案二”);另外一个实验方案不合理的原因: . “方案一”中反应的化学方程式为 .
【答案】
(1)添加液体试剂;锥形瓶
(2)A;CaCO3+2HCl═CaCl2+H2O+CO2↑
(3)铁锈溶解,溶液呈黄色;“方案一”;氯化钙也能与硝酸银反应产生难溶于稀硝酸的白色沉淀;Fe2O3+6HCl═2FeCl3+3H2O
【解析】解:(1)a是长颈漏斗,通常用于添加液体试剂,b是锥形瓶;故填:添加液体试剂;锥形瓶;(2)根据仪器A的特点,当夹上止水夹时,瓶内压强增大,液体被压回长颈漏斗,从而使固液分离,使反应停止,故A可控制反应进行;碳酸钙与稀盐酸反应生成氯化钙、水和二氧化碳;故填:A;CaCO3+2HCl═CaCl2+H2O+CO2↑;(3)取样,加一枚生锈的铁钉,盐酸能与氧化铁反应生成氧化铁和水,铁锈溶解,溶液呈棕黄色;故剩余溶液中一定有盐酸; 取样,滴加AgNO3溶液和稀硝酸,氯化氢和硝酸银反应生成氯化银沉淀,氯化钙也能与硝酸银反应产生难溶于稀硝酸的白色沉淀,故不能确定剩余溶液中一定有盐酸;
稀盐酸与氧化铁反应,生成水和氯化铁溶液,反应的化学方程式是:Fe2O3+6HCl═2FeCl3+3H2O.
所以答案是:铁锈溶解,溶液呈黄色;
“方案一”.氯化钙也能与硝酸银反应产生难溶于稀硝酸的白色沉淀;
Fe2O3+6HCl═2FeCl3+3H2O.
【考点精析】本题主要考查了书写化学方程式、文字表达式、电离方程式的相关知识点,需要掌握注意:a、配平 b、条件 c、箭号才能正确解答此题.

 通城学典默写能手系列答案
通城学典默写能手系列答案 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案