题目内容
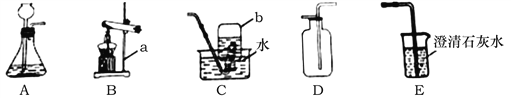
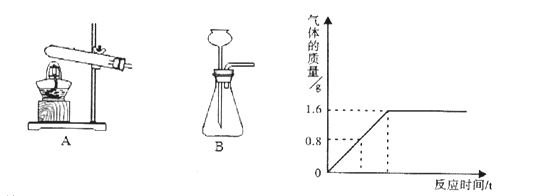
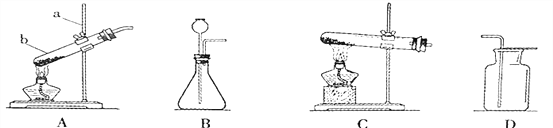
【题目】某化学兴趣小组的同学欲在常温、常压下,用足量的稀硫酸与一定质量的镁反应来测定镁的相对原子质量。利用如下图所示的装置(盛放镁条的隔板有小孔,图中固定装置已略去)进行实验,充分反应后,测得生成氢气的体积为V 。已知本实验条件下,氢气的密度为ρ。关于该实验,有如下说法:
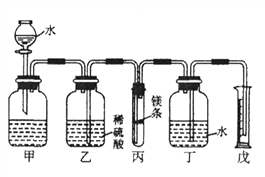
①连接仪器后,要先检查装置的气密性;
②打开分液漏斗的活塞,可观察到乙中稀硫酸进入装置丙中,进入的液体体积对实验结果无影响;
③当丙中无气泡产生时,立即读取量筒戊中水的体积,会使得最终测定结果偏大;
④读取戊中水的体积时仰视读书,会使得最终测定结果偏大;
⑤镁条未反应完全就停止实验,会使得最终测定结果偏大;
⑥利用该实验原理,还可以测定铜的相对原子质量。
其中正确的说法是( )
A. ①④⑥ B. ①②④ C. ②③⑤ D. ①④⑤
【答案】D
【解析】①连接仪器后,要先检查装置的气密性,再装药品,故①正确;②打开分液漏斗的活塞,促使稀硫酸进入装置丙,增大了容器内压强,可观察到乙中稀硫酸进入装置丙中,进入的液体体积偏高,对实验结果有影响,故②错误;③当丙中无气泡产生时,立即读取量筒戊中水的体积,Mg→H2,X→2, ![]() =
=![]() ,X=
,X=![]() M是固定值,m氢气质量偏大,X偏小,会使得最终测定结果偏小,镁与硫酸反应放热,应冷却后再读数比较准确,故③错误;④量筒应平视,读取戊中水的体积时仰视读书,比实际少, Mg→H2,X→2,
M是固定值,m氢气质量偏大,X偏小,会使得最终测定结果偏小,镁与硫酸反应放热,应冷却后再读数比较准确,故③错误;④量筒应平视,读取戊中水的体积时仰视读书,比实际少, Mg→H2,X→2, ![]() =
=![]() ,X=
,X=![]() M是固定值,m氢气质量偏小,X偏大,会使得最终测定结果偏大,故④正确;⑤镁条未反应完全就停止实验,测得的氢气质量偏小,同④一样,会使得最终测定结果偏大,故⑤正确;⑥利用该实验原理,不可以测定铜的相对原子质量,铜与稀硫酸不反应,故⑥错误。故选D。
M是固定值,m氢气质量偏小,X偏大,会使得最终测定结果偏大,故④正确;⑤镁条未反应完全就停止实验,测得的氢气质量偏小,同④一样,会使得最终测定结果偏大,故⑤正确;⑥利用该实验原理,不可以测定铜的相对原子质量,铜与稀硫酸不反应,故⑥错误。故选D。
点睛∶在常温、常压下,可以用足量的稀硫酸与一定质量的镁反应来测定镁的相对原子质量。量筒读数时应平视。

 阅读快车系列答案
阅读快车系列答案