题目内容
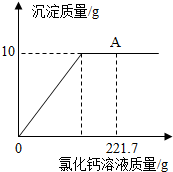 向盛有32.9g碳酸钠和氯化钠固体混合物的烧杯中逐滴加入CaCl2溶液,生成沉淀的质量与滴入CaCl2溶液的质量关系如图所示.反应结束后,A点时溶液中氯化钠溶质的质量分数为26%.(已知:)请计算:
向盛有32.9g碳酸钠和氯化钠固体混合物的烧杯中逐滴加入CaCl2溶液,生成沉淀的质量与滴入CaCl2溶液的质量关系如图所示.反应结束后,A点时溶液中氯化钠溶质的质量分数为26%.(已知:)请计算:(1)原固体混合物中碳酸钠的质量分数.
(2)原固体混合物中钠元素和氯元素的质量比.
考点:根据化学反应方程式的计算,元素质量比的计算
专题:综合计算(图像型、表格型、情景型计算题)
分析:(1)依据碳酸钠和盐酸的反应,利用反应后溶液的氯化钠的溶质质量分数为26%,可以求出碳酸钠的质量;
(2)利用溶液中钠和氯元素的质量分析解答即可;
(2)利用溶液中钠和氯元素的质量分析解答即可;
解答:解:设原固体混合物中碳酸钠的质量是x
Na2CO3+CaCl2=CaCO3↓+2NaCl
106 100 117
x
沉淀的质量为
生成氯化钠的质量为
×100%=26%
x=21.2g
碳酸钠的质量分数为
×100%=64.4%
(2)原混合物固体中氯化钠的质量=(32.9-21.2)g=11.7g
钠元素与氯元素的质量比
=(21.2×
+11.7×
)g:(11.7×
)g
=(9.2+4.6)g:7.1g
=13.8g:7.1g
=138:71
答:原固体混合物中碳酸钠的质量分数为64.4%;原混合物固体中钠元素和氯元素的质量比为138:71.
Na2CO3+CaCl2=CaCO3↓+2NaCl
106 100 117
x
沉淀的质量为
| 100x |
| 106 |
| 117x |
| 106 |
(32.9-x)g+
| ||
32.9g+122.1g-
|
x=21.2g
碳酸钠的质量分数为
| 21.2g |
| 32.9g |
(2)原混合物固体中氯化钠的质量=(32.9-21.2)g=11.7g
钠元素与氯元素的质量比
=(21.2×
| 46 |
| 106 |
| 23 |
| 58.5 |
| 35.5 |
| 58.5 |
=(9.2+4.6)g:7.1g
=13.8g:7.1g
=138:71
答:原固体混合物中碳酸钠的质量分数为64.4%;原混合物固体中钠元素和氯元素的质量比为138:71.
点评:本题较好的考查学生利用图象来分析化学反应的能力,学生应明确图象中的关键点及线的变化所表示的含义,将图象和化学反应紧密结合是解题的关键所在.

练习册系列答案
 课课练江苏系列答案
课课练江苏系列答案 名牌中学课时作业系列答案
名牌中学课时作业系列答案 明天教育课时特训系列答案
明天教育课时特训系列答案 浙江新课程三维目标测评课时特训系列答案
浙江新课程三维目标测评课时特训系列答案
相关题目
下列对实验现象的描述,错误的是( )
| A、镁条在空气中剧烈燃烧,发出耀眼白光 |
| B、向氯化钙溶液中通入二氧化碳,出现大量白色沉淀 |
| C、向稀硫酸中滴加紫色石蕊试液,溶液变成红色 |
| D、硫在空气中燃烧产生微弱的淡蓝色火焰,并生成无色有刺激性气味的气体 |
 小强同学在公共场所围墙上看到一则化肥广告(如图).回校后,小强想通过计算氮的质量分数判断该广告是否为虚假广告.
小强同学在公共场所围墙上看到一则化肥广告(如图).回校后,小强想通过计算氮的质量分数判断该广告是否为虚假广告.
 为了验证鸡蛋壳的成分里含有碳酸盐,小红和小娟进行了如下探究
为了验证鸡蛋壳的成分里含有碳酸盐,小红和小娟进行了如下探究