题目内容
 小强同学在公共场所围墙上看到一则化肥广告(如图).回校后,小强想通过计算氮的质量分数判断该广告是否为虚假广告.
小强同学在公共场所围墙上看到一则化肥广告(如图).回校后,小强想通过计算氮的质量分数判断该广告是否为虚假广告.(1)请你写出小强的计算过程和判断依据.
计算过程:
判断依据
结论:该广告
(2)小强认为此广告会坑害农民,向有关部门反映,技术监督局对该产品取样分析,发现氮元素质量分数仅为28%,则该产品中硝酸铵的质量分数为
考点:元素的质量分数计算
专题:化学式的计算
分析:(1)分析该题可得计算出纯净的硝酸铵中的氨的质量分数,看是否可达38%即可.
(2)可通过设硝酸铵质量为X,总质量为Y,以混合后氮元素的质量分数为28%为等量关系来计算.
(2)可通过设硝酸铵质量为X,总质量为Y,以混合后氮元素的质量分数为28%为等量关系来计算.
解答:解:(1)NH4NO3中氮元素的质量分数为
×100%=35%,35%<38%;该广告是虚假广告;
(2)设NH4NO3质量为X,硝酸铵样品的质量为Y,则得方程式为
=28%,可得
×100%=
×100%=80%,
则该产品中硝酸铵的质量分数为80%.
答案:(1)NH4NO3中氮元素的质量分数为
×100%=35%;35%<38%; 是
(2)80%.
| 28 |
| 14×2+1×4+16×3 |
(2)设NH4NO3质量为X,硝酸铵样品的质量为Y,则得方程式为
| 35%X |
| Y |
| X |
| Y |
| 4 |
| 5 |
则该产品中硝酸铵的质量分数为80%.
答案:(1)NH4NO3中氮元素的质量分数为
| 28 |
| 14×2+1×4+16×3 |
(2)80%.
点评:本题主要考查混合物种某元素的质量计算、化合物中某元素的质量计算以及标签上标示的物质成分及其含量.

练习册系列答案
 轻松课堂单元测试AB卷系列答案
轻松课堂单元测试AB卷系列答案 小题狂做系列答案
小题狂做系列答案
相关题目
水和空气是宝贵的自然资源,下列说法正确的是( )
| A、水在自然界中不断循环,取之不尽、用之不竭 |
| B、水是常见的溶剂,广泛用于工农业生产 |
| C、空气中含量最多的气体是氧气 |
| D、焚烧秸秆不会造成大气污染 |

 用Ba(OH)2溶液测定某种氮肥中(NH4)2SO4的质量分数(杂质溶于水,但不参加反应).实验如下:称取该氮肥20g加水完全溶解,向该溶液中不断滴入Ba(OH)2溶液,生成气体及沉淀质量与加入Ba(OH)2溶液的质量关系如下所示:
用Ba(OH)2溶液测定某种氮肥中(NH4)2SO4的质量分数(杂质溶于水,但不参加反应).实验如下:称取该氮肥20g加水完全溶解,向该溶液中不断滴入Ba(OH)2溶液,生成气体及沉淀质量与加入Ba(OH)2溶液的质量关系如下所示: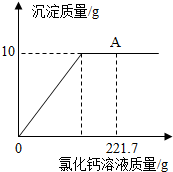 向盛有32.9g碳酸钠和氯化钠固体混合物的烧杯中逐滴加入CaCl2溶液,生成沉淀的质量与滴入CaCl2溶液的质量关系如图所示.反应结束后,A点时溶液中氯化钠溶质的质量分数为26%.(已知:)请计算:
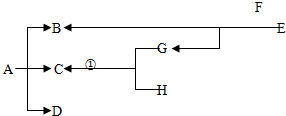
向盛有32.9g碳酸钠和氯化钠固体混合物的烧杯中逐滴加入CaCl2溶液,生成沉淀的质量与滴入CaCl2溶液的质量关系如图所示.反应结束后,A点时溶液中氯化钠溶质的质量分数为26%.(已知:)请计算: (1)A、B、C及甲、乙均为初中化学中常见物质.其中,B为黑色固体,A能结合血红蛋白使人中毒.它们有如图所示的转化关系(“-”表示相互间能反应,“→”表示能转化),部分反应物和生成物及反应条件未标注.请回答:
(1)A、B、C及甲、乙均为初中化学中常见物质.其中,B为黑色固体,A能结合血红蛋白使人中毒.它们有如图所示的转化关系(“-”表示相互间能反应,“→”表示能转化),部分反应物和生成物及反应条件未标注.请回答: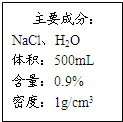 如图是一瓶医用注射盐水标签的部分内容.完成下列填空:
如图是一瓶医用注射盐水标签的部分内容.完成下列填空: