题目内容
【题目】学习化学知识和技能,可以帮助我们鉴别和检验物质。
(1)在实验室鉴别白酒与白醋,可采用的方法是____。
(2)现有两瓶失去标签的无色溶液,其中一瓶是氢氧化钙溶液,一瓶是稀盐酸。为了鉴别它们,同学们设计了如下实验方案:先给两瓶溶液贴上标签A、B,然后分别取样进行实验。请将横线部分填写完整:
加入的试剂 | 现象 | 结论 | |
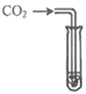
方案1 | 二氧化碳 | A中出现白色浑浊,B中无明显现象。 | A是____溶液, B是另一种溶液。 |
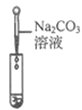
方案2 | 碳酸钠溶液 | _____。 | |
方案3 | 试剂X | …… |
写出方案1中发生反应的化学方程式____。
(方法感悟)在鉴别物质时,要先分析物质的性质,然后选择恰当的试剂,必须产生不同现象才能达到鉴别物质的目的。
(拓展应用)完成方案3,请从下列提供的试剂中选出所有能鉴别出这两种物质的试剂X ____。(填序号)
①酚酞溶液 ②pH试纸 ③镁 ④氧化铜 ⑤稀硝酸 ⑥氢氧化铜 ⑦氯化镁溶液 ⑧硝酸钡溶液
(3)小华同学对方案2进一步探究,设计了如下实验方案:
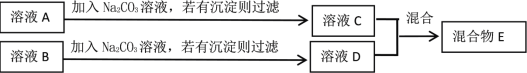
溶液C和溶液D混合,可能会出现以下三种情况:
①有沉淀产生时,写出其中发生反应的化学方程式____。
②有气泡冒出时,可通过现象反推出溶液C中的溶质是____。
③无明显现象时,混合物E中一定含有的溶质的化学式____。
【答案】闻气味 A是Ca(OH)2 A中有白色沉淀生成,B中有气泡冒出 Ca(OH)2 + CO2 = CaCO3↓+ H2O ①②③④⑥⑦(完整给分) Ca(OH)2 + Na2CO3 == CaCO3↓+ 2NaOH Na2CO3和NaOH NaCl
【解析】
(1)在实验室鉴别白酒与白醋,可采用的方法是闻气味,白醋有刺激性酸味,白酒有一种醇香气味;
(2)现有两瓶失去标签的无色溶液,其中一瓶是氢氧化钙溶液,一瓶是稀盐酸。给两瓶溶液贴上标签A、B,然后分别取样进行实验。
加入的试剂 | 现象 | 结论 | |
方案1 | 二氧化碳 | A中出现白色浑浊,B中无明显现象。 | A是Ca(OH)2溶液,,二氧化碳可以使澄清石灰石变浑浊; B是另一种溶液。 |
方案2 | 碳酸钠溶液 | A中有白色沉淀生成,B中有气泡冒出 | |
方案3 | 试剂X | …… |
方案1中发生反应的化学方程式为Ca(OH)2 + CO2 = CaCO3↓+ H2O
[拓展应用] 完成方案3,从提供的试剂中选出所有能鉴别出这两种物质的试剂X应与盐酸或氢氧化钙反应有明显的现象就行,所以除了稀硝酸和硝酸钡外都可以故选:①②③④⑥⑦;
(3)①有沉淀产生时,其中发生反应的方程式为Ca(OH)2 + Na2CO3 == CaCO3↓+ 2NaOH;
②有气泡冒出时,可通过现象反推出溶液C中的溶质是Na2CO3和NaOH
③无明显现象时,混合物E中一定含有的溶质是NaCl

 阅读快车系列答案
阅读快车系列答案【题目】酸、碱、盐是九年级化学学习的重要知识,并且它们具有广泛的用途。
(1)下列关于酸、碱、盐的说法正确的是________________。
A 酸与金属都能反应生成盐和氢气 B 能够生成盐和水的反应都叫做中和反应
C 酸和碱都含有氢元素 D 酸、碱、盐之间都能发生复分解反应
(2)酸和碱之间能够发生中和反应,康康向滴有酚酞的氢氧化钠溶液中逐滴加入稀盐酸,该反应的化学方程式为________________;若滴加一定量稀盐酸后溶液变为无色,测得反应后溶液的 pH=6,则溶液中存在的阳离子为________________ (填离子符号)。
(3)某白色固体中可能含有碳酸钠、硝酸钡、氢氧化钠、硫酸铜中的一种或几种,为确定该固 体成分,现进行以下实验:
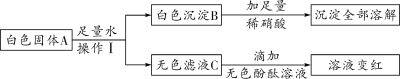
①根据上述实验分析,A 中一定含有的物质是________________,C 中一定含有的溶质是
________________。
②为进一步确定固体 A 中可能存在的物质,对滤液 C 进行实验,完成下表。
实验操作 | 现象 | 结论 |
________________ | ________________ | A中有氢氧化钠 |
(4)将 50 g 稀盐酸加入 50 g 氢氧化钠溶液中恰好完全反应,所得溶液中溶质的质量分数 为 5.85%。试计算氢氧化钠溶液中溶质的质量分数。________________
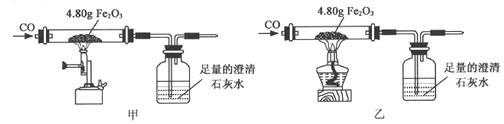
【题目】某学习小组对课本中“食盐常用于制氯气、烧碱”的内容产生兴趣。在老师的指导下,用自制的实验装置(主体部分如下图所示)进行电解饱和食盐水制取氢氧化钠的实验。一段时间后,关闭电源,从K处导出部分的溶液作为待测液进行如下探究。
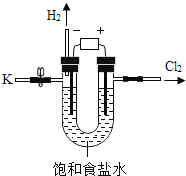
老师提示:
I.电解饱和食盐水的化学方程式:
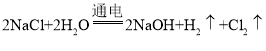
II. 忽略其他可能发生的反应对以下实验的影响。
探究活动一:检验待测液中含有氢氧化钠
(1)同学们选用某种酸碱指示剂对待测液进行检验,请你将实验报告填写完整。
实验步骤 | 实验现象 | 实验结论 |
________ | ________ | 待测液呈碱性,表明含有氢氧化钠 |
探究活动二:测定待测液中氢氧化钠的质量分数
(实验1)用酸碱中和法测定:甲组同学称取一定质量的待测液于烧杯中,加水稀释,用带有刻度的滴管逐滴加入一定溶质质量分数的稀盐酸,边加边振荡,用pH计测定溶液的pH,所得数据如下:
加入稀盐酸的体积/mL | 0 | 2.0 | 4.0 | 6.0 | 8.0 | 9.8 |
烧杯中溶液的pH | 13.0 | 12.9 | 12.8 | 12.6 | 12.3 | 7.0 |
(2)写出氢氧化钠与稀盐酸反应的化学方程式:________________________________。
(3)氢氧化钠与稀盐酸恰好完全反应时共消耗稀盐酸的体积为________mL。
(实验2)用沉淀法测定:
乙组同学按下图所示的实验步骤进行实验:

(4)步骤②加入的氯化镁溶液必需足量,其目的是___________。滴加一定量氯化镁溶液后,判断所加氯化镁溶液是否足量的具体操作:静置,________________________(写出实验步骤、现象和结论)。
(5)步骤③过滤出的沉淀物是________________。
(6)利用沉淀物的质量计算氢氧化钠的质量分数,若缺少步骤④的操作,所测定氢氧化钠的质量分数将________(选填“偏大”、“偏小”或“没影响”)。
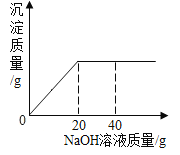
(7)甲组同学称取100g的待测液于烧杯中,向其中边入氯化镁溶液,测得加入氯化镁溶液质量和产生沉淀质量的数据如下:
加入氯化镁溶液的质量/g | 0 | 50 | 100 | 150 | 200 | 250 |
沉淀的质量/g | 0 | 2.9 | 5.8 | m | 11.6 | 11.6 |
①表中m= _____
②则待测液中氢氧化钠的质量分数是________(有计算过程)
【题目】某化学课堂围绕“酸碱中和反应”,将学生分成若干小组开展探究活动。请你和他们一起完成以下实验探究。
【演示实验】将一定量稀盐酸加入到盛氢氧化钙溶液的小烧杯中。该反应的化学方程式是_____________。
【查阅资料】CaC12 滚液显中性
【提出问题】实验中未观察到明显现象,部分同学产生了疑问:反应后溶液中溶质的成分是什么?
【猜想与假设】针对疑问,甲组同学猜想如下:
猜想I:只有CaC12 猜想II:有__________
猜想III:有CaC12和Ca(OH)2 猜想IV:有CaCl2、HCl和Ca(OH)2
乙组同学对以上猜想提出质疑,认为猜想IV不合理,其理由是_________________。
【实验探究】为了验证其余猜想,各小组进行了下列三个方案的探究。
实验方案 | 滴加紫色石蕊溶液 | 通入CO2 | 滴加Na2CO3溶液 |
实验操作 |
|
|
|
实验现象 | ____________ | __________ | 产生白色沉淀 |
实验结论 | 溶液中含有Ca(OH)2 | 溶液中含有Ca(OH)2 | 溶液中含有Ca(OH)2 |
【得出结论】通过探究,全班同学一致确定猜想III是正确的。
【评价反思】(1)丙组同学认为滴加Na2CO3溶液产生白色沉淀,并不能证明溶液中一定含有Ca(OH)2,请你帮助他们说明原因____________。
(2)在分析反应后所得溶液中溶质的成分时,除了考虑生成物外.还需要考虑_______。