题目内容
【题目】能源、环境与人类的生活和社会发展密切相关.
(1)天然气燃烧的化学方程式为;
(2)液氨有望成为新一代绿色能源.氨气在纯氧中燃烧生成空气中含量最多的气体和一种氧化物,且释放大量热量.该反应的化学方程式 .
(3)为节约能源,使燃料充分燃烧,应考虑的因素是(写出一条即可).
【答案】
(1)CH4+2O2 ![]() ?CO2+2H2O
?CO2+2H2O
(2)4NH3+3O2 ![]() ?6H2O+2N2
?6H2O+2N2
(3)一是燃烧时要有足够多的空气;二是燃料与空气要有足够大的接触面积
【解析】解:天然气的主要成份是甲烷,甲烷在燃烧时生成了二氧化碳和水,反应的方程式是:CH4+2O2 ![]() CO2+2H2O;故答为:CH4+2O2
CO2+2H2O;故答为:CH4+2O2 ![]() CO2+2H2O;(2)空气中含量最多的气体是氮气,所以氨气在纯氧中可以完全燃烧,只生成水和氮气,反应的方程式是:4NH3+3O2
CO2+2H2O;(2)空气中含量最多的气体是氮气,所以氨气在纯氧中可以完全燃烧,只生成水和氮气,反应的方程式是:4NH3+3O2 ![]() 6H2O+2N2;故填:4NH3+3O2
6H2O+2N2;故填:4NH3+3O2 ![]() 6H2O+2N2;(3)使燃料充分燃烧可以从增大氧气的浓度或与氧气的接触面积来考虑. 所以答案是:一是燃烧时要有足够多的空气;二是燃料与空气要有足够大的接触面积.
6H2O+2N2;(3)使燃料充分燃烧可以从增大氧气的浓度或与氧气的接触面积来考虑. 所以答案是:一是燃烧时要有足够多的空气;二是燃料与空气要有足够大的接触面积.
【考点精析】认真审题,首先需要了解书写化学方程式、文字表达式、电离方程式(注意:a、配平 b、条件 c、箭号),还要掌握完全燃烧与不完全燃烧(影响燃烧现象的因素:可燃物的性质、氧气的浓度、与氧气的接触面积)的相关知识才是答题的关键.

 阶梯计算系列答案
阶梯计算系列答案【题目】酸和碱的知识是九年级化学学习的重要知识.请回答下列有关问题:
(1)下列说法中不正确的是 . (填字母代号) a.酸和碱都含有氢元素 b.生成盐和水的反应一定是中和反应
c.多数酸和碱有腐蚀性 d.酸和碱能与所有的盐发生复分解反应
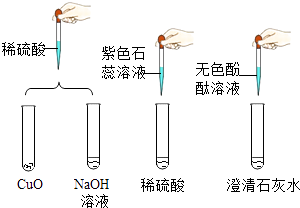
(2)为探究酸、碱的化学性质,某小组做了如图所示实验. ①实验后某试管中为红色溶液,向其中加入一定量的某溶液后,红色消失变为无色,则此时溶液的pH7.该反应的化学方程式为 .
②实验结束后,将得到的蓝色溶液和无色溶液倒入同一个干净的烧杯中,可观察到有蓝色沉淀生成,请解释其原因?
(3)某敞口放置的氢氧化钠溶液已变质,用方程式表示其变质的原因. 为证明该瓶氢氧化钠溶液未完全变质,设计了以下实验,请将表格填写完整.
实验操作 | 现象 | 结论或化学方程式 |
取少量该样品,滴加足量的某溶液,充分反应后过滤 | 有白色沉淀生成 | 有关反应的化学方程式为 |
在滤液中滴加酚酞溶液 | ② | 样品未完全变质,仍含有氢氧化钠 |
(4)取已变质的氢氧化钠溶液100g,向其中加入溶质质量分数为7.3%的稀盐酸100g,恰好完全反应得到中性溶液.试计算蒸干该溶液可得到固体的质量.