题目内容
【题目】结合下图回答问题:
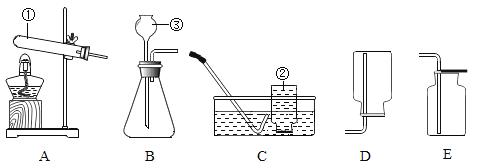
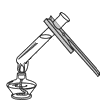
(1)写出图中标有序号仪器的名称 ①_______________③______________
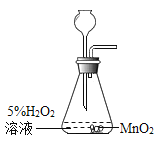
(2)用过氧化氢溶液和二氧化锰制取氧气,反应的化学方程式____________________________,其中二氧化锰起___________作用,若用C装置收集氧气,观察到导气管口气泡_____________,再开始收集。若用E装置收集氧气的验满的方法是_____________。
(3)写出用B装置和适当药品制取气体(O2除外)的一个反应化学方程式______________
【答案】试管 长颈漏斗 2H2O2![]() 2H2O+O2↑ 催化 连续、均匀冒出 将带火星木条放在瓶口,若复燃则满 CaCO3+2HCl=CaCl2+H2O+CO2↑或Zn+H2SO4=ZnSO4+H2↑
2H2O+O2↑ 催化 连续、均匀冒出 将带火星木条放在瓶口,若复燃则满 CaCO3+2HCl=CaCl2+H2O+CO2↑或Zn+H2SO4=ZnSO4+H2↑
【解析】
根据过氧化氢溶液(液体)和二氧化锰(固体)常温下制取氧气、收集、检验的方法进行分析。
(1)仪器的名称①是试管;③是长颈漏斗。
(2)用过氧化氢溶液和二氧化锰制取氧气,反应生成水和氧气,化学方程式2H2O2![]() 2H2O+O2↑ ;其中二氧化锰起催化作用;若用C装置收集氧气,观察到导气管口气泡连续、均匀冒出,再开始收集;用E装置收集氧气的验满的方法是将带火星木条放在瓶口,若复燃则满。
2H2O+O2↑ ;其中二氧化锰起催化作用;若用C装置收集氧气,观察到导气管口气泡连续、均匀冒出,再开始收集;用E装置收集氧气的验满的方法是将带火星木条放在瓶口,若复燃则满。
(3)用B装置和适当药品制取气体(O2除外)的一个反应化学方程式
CaCO3+2HCl=CaCl2+H2O+CO2↑或Zn+H2SO4=ZnSO4+H2↑。

 学而优衔接教材南京大学出版社系列答案
学而优衔接教材南京大学出版社系列答案【题目】氧气具有广泛的用途,某化学小组进行有关氧气制备的探究.
Ⅰ.氧气的制备原理.
(1)工业上利用气体的_____(填“物理”或“化学”)性质不同来分离液态空气制备氧气.
(2)实验室常用过氧化氢溶液、氯酸钾、高锰酸钾等为原料制备氧气,其中氯酸钾制备氧气的化学方程式为_____________________,该反应类型为___________.
(3)植物通过光合作用吸收_______气体,呼出氧气.
Ⅱ.过氧化氢分解速率影响因素探究
小组同学用用数字化实验探究外界条件对过氧化氢分解速率的影响,实验装置如下:
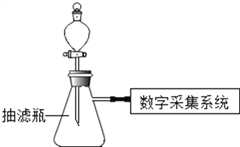
(进行实验)
序号 | 主要实验步骤 | 装置内压强﹣时间图象 |
实 验 1 | ①1号抽滤瓶中不加任何试剂. 2号抽滤瓶中加入0.2gMnO2粉末, 3号抽滤瓶中加入0.2gFeCl3粉末 ②用三支分液漏斗分别加入15mL4%的H2O2溶液 |
|
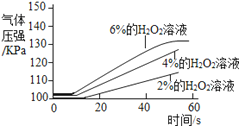
实 验 2 | ①三个抽滤瓶中分别加入0.2g FeCl3粉末 ②分别用1号分液漏斗加入15mL 2%的H2O2溶液;用2号分液漏斗加入15mL 4%的H2O2溶液;用3号分液漏斗加入15mL 6%的H2O2溶液 |
|
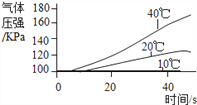
实 验 3 | ①三个抽滤瓶中分别加入0.2g FeCl3粉末 ②_____________________________。 ③_____________________________。 |
|
(结果与分析)
(4)实验1的目的是_____,结论是_____,3号抽滤瓶中发生的化学反应方程式为________________.
(5)实验2可得出过氧化氢的浓度越大,反应速率越快的结论,则图中曲线a代表的溶液是__________________.
(6)通过上述实验可知影响H2O2分解速率的外界因素有_____________.
(反思与评价)
(7)经过多长实验,有的同学对比实验1和3号瓶、实验2的2号瓶中同为40s时的气体压强,发现存在较大的差异,可能的原因是_____.