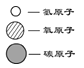
题目内容
【题目】甲、乙、丙、丁是初中化学常见物质。其中甲是单质,乙、丙是组成元素完全相同的两种气体,它们相互转化的关系如图(部分反应物或生成物及反应条件略)。
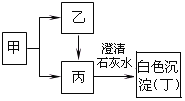
(1)甲物质的化学式是__________;丁物质名称是_____________;
(2)乙和丙组成元素相同,但它们化学性质却有很大差异,原因是什么?
_____________________________________________
(3)请写出由丙转化丁的化学方程式:___________________________________
【答案】C 碳酸钙 分子构成不同(或物质种类不同,合理即可) CO2+Ca(OH)2=CaCO3↓+H2O
【解析】
甲、乙、丙、丁是初中化学常见物质,甲是单质,乙、丙是组成元素完全相同的两种气体,丙和澄清石灰水反应会生成白色沉淀,所以丙是二氧化碳,乙是一氧化碳,甲是碳,二氧化碳和氢氧化钙反应生成碳酸钙沉淀和水,所以丁是碳酸钙,经过验证,推导正确。
由分析可知(1)甲是C,丁是碳酸钙;
(2)二氧化碳和一氧化碳组成元素相同,但它们化学性质却有很大差异,原因是:分子构成不同;
(3)丙转化丁的反应是二氧化碳和氢氧化钙反应生成碳酸钙沉淀和水,化学方程式为:CO2+Ca(OH)2=CaCO3↓+H2O。

 53随堂测系列答案
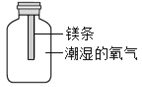
53随堂测系列答案【题目】某兴趣小组为验证质量守恒定律,做了镁条在空气中燃烧的实验。
(1)请写出镁条与氧气反应的化学方程式_____。
(2)小明发现燃烧产物的质量大于反应物镁条的质量,认为这个反应不遵守质量守恒定律。我____(“同意”或“不同意”)小明的观点,因为___。
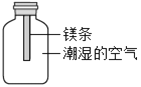
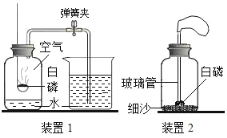
(3)小红按如图装置改进实验,验证了质量守恒定律,却发现产物中还有少量黄色固体。
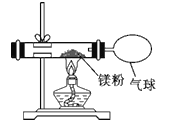
(提出问题)黄色固体是什么呢?
(查阅资料)①氧化镁为白色固体;
②镁能与氮气反应生成黄色的氮化镁(Mg3N2)固体;
③氮化镁可与水剧烈反应产生氨气,该气体能使无色酚酞试液变色。
(做出猜想)黄色固体为Mg3N2
(实验探究)请设计实验,验证猜想
实验操作 | 实验现象 | 结论 |
(1)取样于试管中,加入少量的水 (2)将生成的气体通入到_______中 | 试管中________________ 溶液呈________色。 | 黄色固体为Mg3N2 |
(反思与交流)空气中N2的含量远大于O2的含量,而镁条在空气中燃烧生成的MgO却远多于Mg3N2,为什么呢?请给出合理的解释___。