题目内容
【题目】用化学知识回答下列问题:
(1)在H、O、C、S、Ca、Na六种元素中,选择适当的元素,组成符合下列要求的物质,将其化学式填入空格中。
可用于人工降雨的氧化物________;可用于金属表面除锈的酸_________;
可改良酸性土壤的碱____________;可作干燥剂的氧化物___________。
(2)澄清的饱和石灰水升高温度会变浑浊,原是__________;
澄清的饱和石灰水露置空气中变浑浊,原因是(方程式表示)_________。
(3)小华在实验室帮老师整理药品时,发现一瓶失去标签的白色固体,老师告知是氢氧化钠、硫酸铜、氯化钠、碳酸钙中的一种。小华思考片刻后,认为取少量白色固体放入水中就能确定其成分,她的理由是:(以下用化学式填写)
若不溶于水,则是_________;若溶于水形成蓝色溶液,则是__________;
若溶于水溶液温度升高,则是_____;若溶于水无明显现象且溶液温度基本不变,则是 ______。
【答案】CO2 H2SO4 Ca(OH)2 CaO Ca(OH)2 溶解度随温度的升高而降低 CO2+Ca(OH)2=CaCO3![]() +H2O CaCO3 CuSO4 NaOH NaCl
+H2O CaCO3 CuSO4 NaOH NaCl
【解析】
(1)固态的二氧化碳俗称干冰,常用于人工降雨,化学式为:CO2;由提供的元素组成的硫酸能与氧化铁反应,所以可用来除锈,化学式为:H2SO4;由提供的元素组成的氢氧化钙常用来改良酸性土壤,化学式为:Ca(OH)2;氧化钙能与水反应,可用作干燥剂,化学式为:CaO;
(2)温度升高,氢氧化钙因溶解度减小而析出,故澄清的饱和石灰水升高温度会变浑浊;氢氧化钙与二氧化碳反应生成难溶性的碳酸钙,故澄清的饱和石灰水露置空气中变浑浊,反应的化学方程式为:CO2+Ca(OH)2=CaCO3![]() +H2O;
+H2O;
(3)不同的物质在水中的溶解情况不同,物质溶于水的不同现象;在原物质中只有碳酸钙不溶于水,其它均能溶于水,化学式为:CaCO3;硫酸铜溶于水溶液呈蓝色,其它溶液均为无色,化学式为:CuSO4;其中氢氧化钠溶于水放热,其它溶于水均无热量变化,化学式为:NaOH;溶于水温度不变的无色溶液是氯化钠,化学式为:NaCl。

 阅读快车系列答案
阅读快车系列答案【题目】物质丙是重要的化工产品,在国民经济中占有重要地位。工业上用甲和乙合成丙。甲、乙、丙的微观示意图见下表。请完成下列空白。
物质 | 甲 | 乙 | 丙 |
|
微观示意图 |
|
|
|
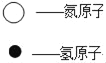
(1)甲、乙、丙3种物质都是由 (填“分子”“原子”或“离子”)_____构成的。
(2)甲、乙、丙中属于化合物的是_____。
(3)物质丙中氮元素的化合价为_____。
(4)丙中氮、氢元素的质量比为_____。
(5)写出甲和乙在高温、高压、催化剂的条件下合成丙的化学方程式:_____。