题目内容
【题目】将5%的NaOH溶液逐滴加入到10g稀硫酸中,边加边搅拌,随着NaOH溶液的加入,溶液pH的变化如图所示.边回答:
(1)a点的含义是 ;
(2)当计入NaOH溶液的质量为18g时,溶液中存在的阴离子有 ;
(3)计算稀硫酸中溶质的质量分数.
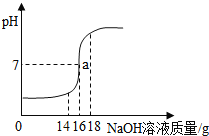
【答案】(1)当加入NaOH溶液的质量为16g时,硫酸与氢氧化钠恰好完全中和;
(2)硫酸根离子与氢氧根离子;(3)9.8%,
【解析】
试题分析:a点pH=7,说明当加入NaOH溶液的质量为16g时,酸碱刚好中和;由图可知,NaOH溶液的质量为18g时,碱过量,溶质是硫酸钠和氢氧化钠,阴离子为硫酸根离子和氢氧根离子;
16gNaOH溶液中溶质的质量为,16g×5%=0.8g
设10g稀硫酸中溶质的质量为x,则
H2SO4+2NaOH=Na2SO4+2H2O
98 80
X 0.8g
98/80=x/0.8g得x=0.98g
稀硫酸中溶质的质量分数=0.98g÷10g×100%=9.8%

练习册系列答案
相关题目