题目内容
在托盘天平的左、右两盘上各放1只烧杯,分别注入等质量且溶质质量分数相同的稀盐酸,调整天平平衡.向左盘烧杯中投入一定质量的CaCO3粉末,向右盘烧杯中投入与CaCO3等质量的MgCO3粉末,充分反应.
若反应后天平失去平衡,那么,天平的指针一定偏向________(填“左”或“右”)
左
分析:计算相同质量的CaCO3和MgCO3完全反应放出二氧化碳质量的大小,分析天平指针的偏转;
天平的指针会偏向质量大(下沉)的一方.
解答:假设两物质质量均为mg,设mgCaCO3反应放出二氧化碳质量为x,mgMgCO3反应放出二氧化碳质量为y
CaCO3+2HCl=CaCl2+H2O+CO2↑
100 44
mg x
100:44=mg:x
解之得 x=
MgCO3+2HCl=MgCl2+H2O+CO2↑
84 44
mg y
84:44=mg:y
解之得 y=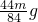
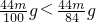 ,即等质量的两种碳酸盐完全反应,MgCO3产生的气体二氧化碳多,
,即等质量的两种碳酸盐完全反应,MgCO3产生的气体二氧化碳多,
则加入MgCO3的天平右端上升,左端下沉;天平指针偏向左端;
故答:左.
点评:等质量的CaCO3和MgCO3,MgCO3中碳酸根的质量分数大,所以完全反应放出二氧化碳气体质量大.
分析:计算相同质量的CaCO3和MgCO3完全反应放出二氧化碳质量的大小,分析天平指针的偏转;
天平的指针会偏向质量大(下沉)的一方.
解答:假设两物质质量均为mg,设mgCaCO3反应放出二氧化碳质量为x,mgMgCO3反应放出二氧化碳质量为y
CaCO3+2HCl=CaCl2+H2O+CO2↑
100 44
mg x
100:44=mg:x
解之得 x=

MgCO3+2HCl=MgCl2+H2O+CO2↑
84 44
mg y
84:44=mg:y
解之得 y=
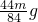
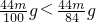 ,即等质量的两种碳酸盐完全反应,MgCO3产生的气体二氧化碳多,
,即等质量的两种碳酸盐完全反应,MgCO3产生的气体二氧化碳多,则加入MgCO3的天平右端上升,左端下沉;天平指针偏向左端;
故答:左.
点评:等质量的CaCO3和MgCO3,MgCO3中碳酸根的质量分数大,所以完全反应放出二氧化碳气体质量大.

练习册系列答案
 亮点激活精编提优100分大试卷系列答案
亮点激活精编提优100分大试卷系列答案
相关题目