题目内容
(1)在相同温度和相同体积的条件下,气体压强与气体分子数目成正比.若a g 碳和b g 氧气放入一密闭容器中,提供一定条件使容器内的物质发生充分反应,待温度复原时,测得容器内的气体压强在反应前后不变.则
(填>、<、≤、≥).
(2)将30℃时含有某种溶质的溶液136克,分成两等份,其中一份加入该溶质10克,结果只溶解2克就不再溶解了;将另一份冷却到0℃时,析出溶质5.5克,此时溶液的溶质质量分数为20%,则该物质在30℃时的溶解度为 .
(3)在托盘天平的左、右两托盘中各放一只烧杯,调节至平衡,向烧杯分别注入等质量、等质量分数的稀硫酸,然后向两只烧杯中分别加入相同质量的镁和铜铝合金,两烧杯中物质完全反应后,天平仍保持平衡,合金中铝与铜的质量比是 .
| a |
| b |
| 3 |
| 8 |
(2)将30℃时含有某种溶质的溶液136克,分成两等份,其中一份加入该溶质10克,结果只溶解2克就不再溶解了;将另一份冷却到0℃时,析出溶质5.5克,此时溶液的溶质质量分数为20%,则该物质在30℃时的溶解度为
(3)在托盘天平的左、右两托盘中各放一只烧杯,调节至平衡,向烧杯分别注入等质量、等质量分数的稀硫酸,然后向两只烧杯中分别加入相同质量的镁和铜铝合金,两烧杯中物质完全反应后,天平仍保持平衡,合金中铝与铜的质量比是
分析:(1)由于反应前后容器内气体压强不变,根据在相同温度和相同体积的条件下,气体压强(P)与气体分子数目(n)成正比关系(P=kn),可判断反应前后气体的分子数目没改变;根据碳在氧气中充分燃烧与不充分燃烧的规律,此时碳应充分燃烧全部生成二氧化碳,其中氧气足量或过量;根据碳在氧气中完全燃烧的化学方程式,由反应中碳与所消耗氧气的质量关系,判断密闭容器中ag碳和bg氧气的关系;
(2)由溶液中溶质的质量分数=
×100%,可得溶质的质量=溶液的质量×溶质的质量分数,溶液在降温析出晶体的过程中只是溶质的质量发生变化,溶剂的质量并没有发生变化;再由溶剂质量和溶质质量计算溶解度;
(3)该题目将化学反应与托盘天平平衡结合在一起.两盘中酸和金属质量相等,完全反应,天平仍平衡则产生氢气相等.由氢气质量求出反应的铝和镁的质量进而求出铜的质量.
(2)由溶液中溶质的质量分数=
| 溶质质量 |
| 溶液质量 |
(3)该题目将化学反应与托盘天平平衡结合在一起.两盘中酸和金属质量相等,完全反应,天平仍平衡则产生氢气相等.由氢气质量求出反应的铝和镁的质量进而求出铜的质量.
解答:解:(1)解:根据题意,反应前后分子数目不变,由C+O2
CO2与2C+O2
2CO,可判断碳在氧气中充分燃烧生成二氧化碳,
假设ag碳和bg氧气恰好完全反应,则
C+O2
CO2
12 32
ag bg
=
则
=
若容器中氧气有剩余,反应前后分子数目也不变,反应前后压强也相同,因此,容器中碳的质量与氧气的质量
<
,所以
≤
;故填:≤;
(2)将136克溶液分成两份,即每份68克,将其中一份冷却至0℃,析出5.5g溶质,则溶液还有68g-5.5g=62.5g,
溶液中的溶质是62.5g×20%=12.5g,
则68克溶液在未降温之前的溶质质量为:12.5g+5.5g=18g,溶剂质量为:68g-18=50g;
加入溶质10g,只溶2g就不溶解,说明已达饱和,此时溶液中溶质质量为:18g+2g=20g;
即30℃时,在50故g水中溶解20g该物质达到饱和.
物质在30℃时的溶解度为S,
=
解之得:S=40g;故填:40g;
(3)设产生氢气的质量为2,需要镁的质量为x,需要铝的质量为y,则有
Mg+H2SO4═MgSO4+H2↑
24 2
x 2
=
x=24
2Al+3H2SO4═Al2(SO4)3+3H2↑
54 6
y 2
=
y=18
铜铝合金的质量与镁的质量相等,故铜的质量为24-18=6,所以铝和铜的质量比为18:6=3:1.故填:3:1.
| ||
| ||
假设ag碳和bg氧气恰好完全反应,则
C+O2
| ||
12 32
ag bg
| 12 |
| ag |
| 32 |
| bg |
则
| a |
| b |
| 3 |
| 8 |
若容器中氧气有剩余,反应前后分子数目也不变,反应前后压强也相同,因此,容器中碳的质量与氧气的质量
| a |
| b |
| 3 |
| 8 |
| a |
| b |
| 3 |
| 8 |
(2)将136克溶液分成两份,即每份68克,将其中一份冷却至0℃,析出5.5g溶质,则溶液还有68g-5.5g=62.5g,
溶液中的溶质是62.5g×20%=12.5g,
则68克溶液在未降温之前的溶质质量为:12.5g+5.5g=18g,溶剂质量为:68g-18=50g;
加入溶质10g,只溶2g就不溶解,说明已达饱和,此时溶液中溶质质量为:18g+2g=20g;
即30℃时,在50故g水中溶解20g该物质达到饱和.
物质在30℃时的溶解度为S,
| 100g |
| S |
| 50g |
| 20g |
解之得:S=40g;故填:40g;
(3)设产生氢气的质量为2,需要镁的质量为x,需要铝的质量为y,则有
Mg+H2SO4═MgSO4+H2↑
24 2
x 2
| 24 |
| x |
| 2 |
| 2 |
x=24
2Al+3H2SO4═Al2(SO4)3+3H2↑
54 6
y 2
| 54 |
| y |
| 6 |
| 2 |
y=18
铜铝合金的质量与镁的质量相等,故铜的质量为24-18=6,所以铝和铜的质量比为18:6=3:1.故填:3:1.
点评:金属与酸反应后天平平衡的问题是中考常考查的题目,完成此类题目,要分清题干提供的信息,确定是根据酸还是金属的质量进行求算.

练习册系列答案
 出彩同步大试卷系列答案
出彩同步大试卷系列答案
相关题目
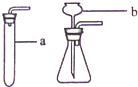 (2007?广州)温室效应已引起全球广泛关注.某校研究小组的同学在中学生“我与化学”活动中,为了研究空气中CO2含量对空气温度的影响,进行了下列实验:
(2007?广州)温室效应已引起全球广泛关注.某校研究小组的同学在中学生“我与化学”活动中,为了研究空气中CO2含量对空气温度的影响,进行了下列实验: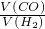 ═______;
═______; ═______;
═______;