题目内容
高铁酸钾(K2FeO4)是红黑色粉末,小晶体呈现红彩闪光,易溶于水,易与水反应,干燥的高铁酸钾在198℃以下是稳定的,受热易分解.根据上述信息,请回答下列问题:
(1)高铁酸钾中铁元素的化合价
(2)保存高铁酸钾时应注意
(3)试完成化学反应方程式4K2FeO4+10H2O=4Fe(OH)3↓+8KOH+ ↑
(1)高铁酸钾中铁元素的化合价
(2)保存高铁酸钾时应注意
(3)试完成化学反应方程式4K2FeO4+10H2O=4Fe(OH)3↓+8KOH+
考点:有关元素化合价的计算,化学性质与物理性质的差别及应用,质量守恒定律及其应用
专题:结合课本知识的信息
分析:根据题干提供的信息进行分析,化合物中各元素正负化合价的代数和为零,在化学反应前后,元素的种类和原子的个数不变来确定化学式.
解答:解:(1)设铁元素的化合价为x,则有,(+1)+x+(-2)×4=0,解得x=+6,故填:+6;
(2)高铁酸钾易溶于水且与水反应,需要密封保存,干燥的高铁酸钾在受热时易分解,需要低温保存,故填:密封、放在低温处;
(3)根据反应的化学方程式可以知道,反应前有8个钾原子,4个铁原子,20个氢原子,26个氧原子,反应后有8个钾原子,4个铁原子,20个氢原子,30个氧原子,故生成的气体为氧气,且分子个数为3,故填:3O2.
(2)高铁酸钾易溶于水且与水反应,需要密封保存,干燥的高铁酸钾在受热时易分解,需要低温保存,故填:密封、放在低温处;
(3)根据反应的化学方程式可以知道,反应前有8个钾原子,4个铁原子,20个氢原子,26个氧原子,反应后有8个钾原子,4个铁原子,20个氢原子,30个氧原子,故生成的气体为氧气,且分子个数为3,故填:3O2.
点评:本题考查了化合价的求算以及物质间反应的化学方程式,完成此题,可以依据化合价规则和题干提供的信息进行.

练习册系列答案
相关题目
“环境保护,以人为本”从2000年6月起,新调整的空气质量指标中指出,影响空气质量的一组主要污染物是( )
| A、二氧化硫、二氧化氮、可吸入颗粒物 |
| B、二氧化硫、氧气、二氧化碳 |
| C、二氧化碳、氮气、氧气 |
| D、二氧化氮、氮气、可吸入颗粒 |
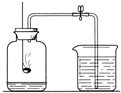 如图,用红磷燃烧来测定空气中氧气含量.
如图,用红磷燃烧来测定空气中氧气含量.