题目内容
【题目】“微观—宏观—符号”三重表征是化学独特的表示物质及其变化的方法。
(1)在石墨、干冰、硫酸铜三种物质中,由分子构成的物质是___________(填化学式)。
(2)根据如图的信息回答问题:
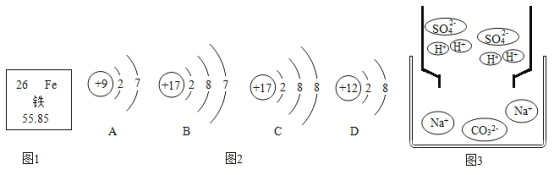
①图1中铁元素的相对原子质量是__________;铁原子失去3个电子形成离子的名称为__________。
②图2中,A、B粒子化学性质相似的主要原因是___________;D 元素位于周期表第___________周期。
C、D两种元素形成化合物的化学式__________。
(3)图3是碳酸钠溶液和稀硫酸反应的微观示意图该反应的微观实质是____________,反应后所得溶液中的溶质是___________(填化学式)。
【答案】CO2 55.85 铁离子 最外层电子数相同 三 MgCl2 H++CO32-→ H2O+CO2↑ Na2SO4、H2SO4
【解析】
(1)石墨由原子构成,干冰由分子构成,硫酸铜由离子构成,故为CO2;
(2)由图1可知,铁元素的相对原子质量是55.85,铁原子失去3个电子形成离子的名称为铁离子;
(3)A、B粒子化学性质相似的主要原因是最外层电子数相同。原子核外电子层数等于周期数,故D 元素位于周期表第三周期。C是氯元素,D是镁元素,形成化合物为MgCl2;
(4)碳酸钠溶液和稀硫酸反应的微观实质是:H++CO32-→ H2O+CO2↑,反应后所得溶液中的溶质是Na2SO4、H2SO4。

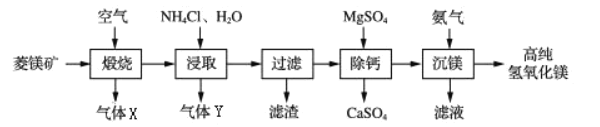
【题目】我国化学家侯德榜改革了国外的纯碱生产工艺,发明了联合制碱法,其生产流程可简要表示如下:
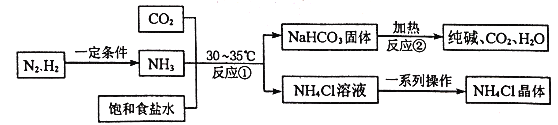
已知![]() 受热易分解,请回答下列问题。
受热易分解,请回答下列问题。
(1)上述流程中可循环利用的物质是________(写一种)
(2)反应②的化学方程式是____________。
(3)下表是几种物质在不同温度下的溶解度。
温度 | 0℃ | 10℃ | 20℃ | 30℃ | 40℃ | 50℃ | 60℃ | 100℃ | |
溶解度/g | NaCl | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 | 37.3 | 39.8 |
| 11.9 | 15.8 | 21.0 | 27.0 | - | - | - | - | |
| 6.9 | 8.2 | 9.6 | 11.1 | 12.7 | 14.5 | 16.4 | - | |
| 29.4 | 33.3 | 37.2 | 41.4 | 45.8 | 50.4 | 55.2 | 77.3 | |
分析表中数据可知,反应①中![]() 作为固体析出的原因是________。上述流程中得到的NH4Cl溶液中一定有_____杂质,经一系列操作后,从
作为固体析出的原因是________。上述流程中得到的NH4Cl溶液中一定有_____杂质,经一系列操作后,从![]() 溶液中获得
溶液中获得![]() 晶体的方法是________。
晶体的方法是________。
【题目】下表是硝酸钾和氯化铵在不同温度时的溶解度。分析表中数据,回答问题。
温度/℃ | 0 | 20 | 40 | 60 | |
溶解度/g | KNO3 | 13.3 | 31.6 | 63.9 | 110 |
NH4Cl | 29.4 | 37.2 | 45.8 | 55.2 | |
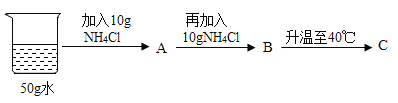
(1)上述下图中,甲可表示________的溶解度曲线。
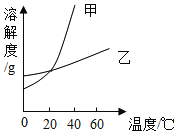
(2)60℃时,两种物质的饱和溶液中,溶质质量分数较小的是_____________。
(3)20℃时,按下图所示操作:B中的溶液是________(选填“饱和”或“不饱和”)溶液,C中溶液的溶质和溶剂质量比为_______。