题目内容
【题目】下表是硝酸钾和氯化铵在不同温度时的溶解度。分析表中数据,回答问题。
温度/℃ | 0 | 20 | 40 | 60 | |
溶解度/g | KNO3 | 13.3 | 31.6 | 63.9 | 110 |
NH4Cl | 29.4 | 37.2 | 45.8 | 55.2 | |
(1)上述下图中,甲可表示________的溶解度曲线。
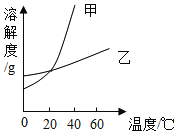
(2)60℃时,两种物质的饱和溶液中,溶质质量分数较小的是_____________。
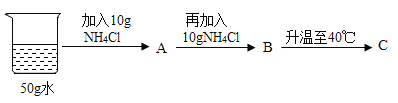
(3)20℃时,按下图所示操作:B中的溶液是________(选填“饱和”或“不饱和”)溶液,C中溶液的溶质和溶剂质量比为_______。
【答案】KNO3或硝酸钾 NH4Cl或氯化铵 饱和 2:5
【解析】
(1)甲的溶解度随温度变化较大,比较硝酸钾和氯化铵在各个温度下的溶解度,可知0℃时,20℃时,硝酸钾溶解度都比氯化铵溶解度小,结合图像,甲可表示硝酸钾的溶解度曲线。
(2)饱和溶液的溶质质量分数为:![]() ,故比较饱和溶液的质量分数,比较该温度下的溶解度即可。60℃时,硝酸钾的溶解度大于氯化铵溶解度,故两种物质的饱和溶液中,溶质质量分数较小的是氯化铵。
,故比较饱和溶液的质量分数,比较该温度下的溶解度即可。60℃时,硝酸钾的溶解度大于氯化铵溶解度,故两种物质的饱和溶液中,溶质质量分数较小的是氯化铵。
(3)20℃时氯化铵的溶解度为37.2g,即该温度下100g水中最多溶解氯化铵37.2g,50g水中最多溶解18.6g,故A是不饱和溶液,B是饱和溶液,根据溶解度表,40℃时,50g水中最多溶解22.9g,故加入的20g溶质能全部溶解,则溶液的溶质和溶剂质量比为20:50=2:5。

 暑假衔接教材期末暑假预习武汉出版社系列答案
暑假衔接教材期末暑假预习武汉出版社系列答案 假期作业暑假成长乐园新疆青少年出版社系列答案
假期作业暑假成长乐园新疆青少年出版社系列答案【题目】食品营养与安全关系到每个人的身体健康。
(1)豆浆已成为众多家庭的早餐选择,下表是豆浆中部分成分的平均含量。
成分 | 水 | 蛋白质 | 脂肪 | 糖类 | 钙 | 磷 | 铁 | 维生素 |
平均含量(%) | 96.0 | 1.8 | 0.7 | 1.1 | 0.01 | 0.03 | 0.0005 | 0.015 |
豆浆的成分中能作为机体生长、修补受损组织的原料的是________,人体缺少表中的________元素会引起贫血。
(2)霉变的花生中含有黄曲霉毒素(化学式![]() )食用后可导致癌症。黄曲霉毒素中碳、氢、氧元素的质量比是________。
)食用后可导致癌症。黄曲霉毒素中碳、氢、氧元素的质量比是________。
【题目】下列方案设计不能达到实验目的的是( )
选项 | 物质 | 目的 | 主要实验操作 |
A |
| 除杂 | 先通过 |
B |
| 分离 | 溶解、过滤、洗涤、干燥、蒸发 |
C |
| 检验是否变质 | 取样,滴加足量稀盐酸,观察现象 |
D |
| 比较活动性 |
|
A.AB.BC.CD.D