题目内容
【题目】一种由菱镁矿(主要成分![]() )制备高纯氢氧化镁的工艺如下:
)制备高纯氢氧化镁的工艺如下:
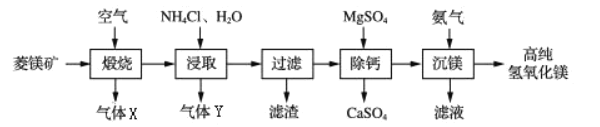
(1)气体X是________________。
(2)“浸取”发生的反应方程式之一为:![]() 。则X的化学式为_______________。“浸取”时控制温度为100℃左右,
。则X的化学式为_______________。“浸取”时控制温度为100℃左右,![]() 用量对
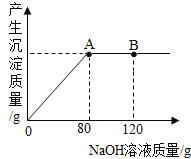
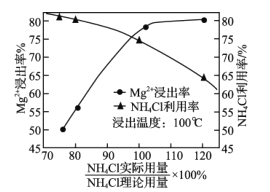
用量对![]() 浸出率的影响曲线如图所示。下列有关说法正确的是________________(填序号)。
浸出率的影响曲线如图所示。下列有关说法正确的是________________(填序号)。
A“浸取”时适当搅拌浆料
B用超理论用量![]() 的
的![]() 进行浸取
进行浸取
C浸出温度采用![]() 可促进
可促进![]() 的逸出
的逸出
(3)“浸取”时体系温度会___________(填“升高”或“降低”),此时,用水量不能太多的主要原因是_____________。
(4)过滤用到的玻璃仪器是___________、玻璃棒、漏斗,过滤时发现所得滤液仍然浑浊,可能的原因是____________。
(5)本工艺流程中可循环利用的物质有![]() 和____________。
和____________。
(6)若要得到高纯![]() ,还需对
,还需对![]() 沉淀进行洗涤,证明沉淀洗净需要的试剂是____________(填写名称)。
沉淀进行洗涤,证明沉淀洗净需要的试剂是____________(填写名称)。
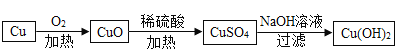
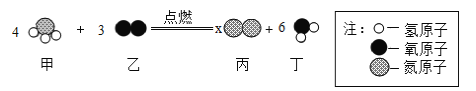
【答案】![]()
![]() AC 升高 氨气能溶于水 烧杯 滤纸破或滤液高于滤纸边缘或仪器不干净 NH3和NH4Cl 氯化钡溶液
AC 升高 氨气能溶于水 烧杯 滤纸破或滤液高于滤纸边缘或仪器不干净 NH3和NH4Cl 氯化钡溶液
【解析】
(1)碳酸钙在高温的条件下生成氧化钙和二氧化碳,碳酸镁在高温的条件下生成氧化镁和二氧化碳,所以气体X是二氧化碳;
(2)化学反应前后,元素种类不变,原子个数不变,反应物中有1个镁原子,1个氧原子,2个氮原子,8个氢原子,2个氯原子,生成物中有1个镁原子,2个氯原子,2个氮原子,6个氢原子,所以X是H2O;
A、搅拌可以加速溶解,加速反应,故A正确;
B、图中看出,用超理论用量20%的NH4Cl进行浸取,镁离子的浸出率基本维持在理论用量,而NH4Cl的利用率反而降低,故B错误;
C、水解反应是吸热反应,适当升高温度可以促进水解,浸取过程产生氨气,温度适当升高,有利于氨气的排出,故C正确。故选AC;
(3)氧化钙与水反应放出热量,所以 “浸取”时体系温度会升高,此时用水量不能太多的主要原因是:氨气溶于水,若水量多时,不易逸出;
(4)过滤用到的玻璃仪器是:烧杯、漏斗、玻璃棒,过滤时发现所得滤液仍然浑浊,可能的原因是:滤纸破或滤液高于滤纸边缘或仪器不干净;
(5)浸取产生的氨气,在沉镁操作中可以使用;沉镁过程,通入氨气,产生氢氧化镁沉淀和氯化铵溶液,产生的氯化铵可以在浸取操作中使用,所以本工艺流程中可循环利用的物质有 NH4Cl 和氨气;
(6)硫酸根离子和钡离子反应会生成硫酸钡沉淀,所以要得到高纯 Mg(OH)2,还需对 Mg(OH)2 沉淀进行洗涤,证明沉淀洗净需要的试剂是氯化钡溶液。

【题目】下列方案设计不能达到实验目的的是( )
选项 | 物质 | 目的 | 主要实验操作 |
A |
| 除杂 | 先通过 |
B |
| 分离 | 溶解、过滤、洗涤、干燥、蒸发 |
C |
| 检验是否变质 | 取样,滴加足量稀盐酸,观察现象 |
D |
| 比较活动性 |
|
A.AB.BC.CD.D