题目内容
【题目】分液漏斗是化学实验室一种常用的仪器,可用于滴加液体或分离互不相溶的两种液体,请根据图回答下列问题:
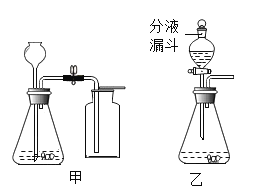
(1)如图甲是实验室制取CO2的装置,实验中收集集满一瓶CO2后,应将盖有玻璃片的集气瓶_____(选填“正放”或“倒放”)在桌面上。
(2)某同学对图甲中的气体发生装置进行了改进,改装后的装置如图乙所示,也可用注射器代替分液漏斗。在实验中可选用生活用品代替一些化学仪器的一个实例为_____。
【答案】正放 眼药水瓶代替滴管(或吸管代替导管,注射器代替量筒,塑料盆代替水槽等)
【解析】
(1)二氧化碳的密度比空气的大,实验中收集满一瓶CO2后,应将盖有玻璃片的集气瓶正放在桌面上。
(2)生活用品中眼药水瓶代替滴管,吸管代替导管,注射器代替量筒,塑料盆代替水槽等。

【题目】已知某种铸造钢轨的金属粉末原料中可能含有铁、锰、铜三种金属中的两种或三种,化学小组的同学对该粉末进行探究
(1)提出猜想:
猜想Ⅰ:该粉末由铜、锰组成
猜想Ⅱ:该粉末由铁、锰组成
猜想Ⅲ:1该粉末由铁、锰、铜组成
猜想Ⅳ:该粉末由____________组成。
(2)查阅资料:金属锰、铜不能被磁铁吸引,锰和硫酸亚铁溶液可以发生置换反应锰元素在生成物中显+2价,生成物的溶液为浅粉色。
(3)进行实验
实验目的 | 实验操作 | 实验现象 |
①证明粉末中是否含有铜 | 取一个小烧杯,加入适量的粉末,再向其中加入过量的___________。 | 有少量红色粉末不能溶解 |
②证明粉末中是否含有锰 | 取5.5g的粉末放入烧杯,再向其中加入过量的硫酸亚铁溶液,反应完全后过滤、干燥、称量固体为5.52g | _____ |
③证明粉末中是否含有铁 | 另取5.5g粉末___________(用物理方法),剩余金属粉末的质量为1.12g | _____ |
(4)初步结论:猜想_______成立,写出实验①中发生反应的一个化学反应方程式为_________________。
(5)数据处理:试计算粉末原料中任意一种金属所占的质量分数____________(用金属的名称和百分数表示,结果保留一位小数)。
【题目】某化学兴趣活动小组的同学为探究影响化学反应速率的因素,在实验室制取二氧化碳的研究中,进行了如下实验:
1 | 甲 | 乙 | 丙 | 丁 |
大理石 | m克,块状 | m克,块状 | m克,粉末状 | m克,粉末状 |
盐酸(过量) | w克,稀盐酸 | w克,浓盐酸 | w克,稀盐酸 | w克,浓盐酸 |
(1)若要研究盐酸浓度大小对反应速率的影响,可选择实验甲与实验______(选填实验编号)进行对照实验。
(2)若要研究反应物的接触面积对反应速率的影响,可选择实验甲与实验___________(选填实验编号)进行对照实验。
(3)乙和丁相比较,产生气体的速率较快的是_________,完全反应后,产生二氧化碳的质量__________(填“相等”或“不等”)。
(4)若要选择丁组药品制取二氧化碳,为了能得到较平稳的气流,应选择如图装置中的______(填“A”或“B”)。由于浓盐酸具有强烈的挥发性,会导致收集到的二氧化碳中含有氯化氢气体,为了得到干燥、纯净的二氧化碳,可将产生的二氧化碳依次通过下列装置_________。(温馨提示:①浓硫酸具有吸水性,可作干燥剂;②二氧化碳不与饱和NaHCO3溶液反应,氯化氢可与之反应,相应的化学方程式:![]() )
)