题目内容
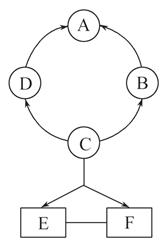
(4分)已知A、B、C、D、E是初中化学中常见的五种物质.其中A、D是黑色固体,B、C、E是无色气体,B和C组成元素相同,化合物D中含有金属元素,该金属元素的单质是世界年产量最高的金属.它们在一定条件下的转化关系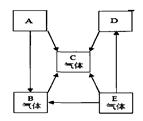
如上图所示(→表示转化).请回答下列问题:
(1)A物质是
(2)评价物质C的“利”与“弊”(各写一例)
利: 弊:
(3)写出D转化为C的化学方程式:
(1)C;(2)是植物光合作用的原料;能造成温室效应;(3)CO+ CuO 加热 Cu + CO2
解析试题分析:由题中的叙述可知A为碳,B为一氧化碳,C为二氧化碳,D氧化铜等金属氧化物,E为氧气,故得到(1)A物质是碳单质;(2)物质C为二氧化碳,对人类有的一面是是植物光合作用的原料,不利的一面为能造成温室效应;(3)D转化为C的化学方程式:CO+ CuO 加热 Cu + CO2
考点:物质的转化和推断

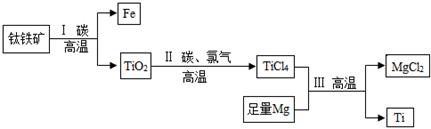
(11分)废铁屑的主要成份是铁,同时还有少量铁锈(Fe2O3),动物饲料硫酸亚铁的生产工艺之一如下图所示: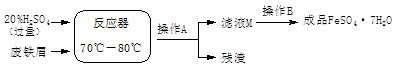
(1)在反应器中发生反应的化学方程式除Fe2(SO4)3+Fe=3FeSO4外还有: ; 。
(2)滤液M中肯定含有的溶质的化学式是 ;
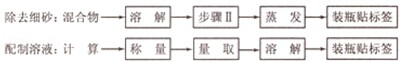
(3)在实验室中完成操作A的玻璃仪器有玻璃棒、烧杯和 ;
(4)滤液M经过操作B可得硫酸亚铁晶体(FeSO4·7H2O)。已知硫酸亚铁的溶解度和析出晶体的组成如下表:
| 温度/℃ | 0 | 10 | 30 | 40 | 50 | 60 | 64 | 70 | 80 | 90 |
| 溶解度/g | 15.6 | 20.5 | 33.0 | 40.4 | 48.8 | 55.0 | 55.3 | 50.6 | 43.7 | 37.2 |
| 析出晶体 | FeSO4·7H2O | FeSO4·4H2O | FeSO4·H2O | |||||||
(5)在化学反应中,若有元素化合价变化的反应定义为氧化还原反应。下列反应类型肯定是氧化还原反应的是 (填字母编号);
A.化合反应 B.置换反应 C.分解反应 D.复分解反应
在氧化还原反应中,若有元素的化合价升高,必有元素的化合价降低,且元素化合价升降总数相等。
将无水硫酸亚铁(FeSO4)隔绝空气加强热,分解产物有三氧化二铁和另两种氧化物,试写出该反应的化学方程式 。
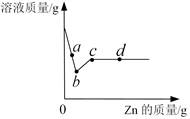
兴趣小组的同学学习了金属的性质后,在实验室找到的一种银白色金属R做如下探究:
(1)将金属R投入稀盐酸中,金属表面有气泡冒出.则该金属R在金属活动性顺序表中排在氢的 (选填“前面”或“后面”)。
(2)为了比较金属R与铁的活动性强弱,兴趣小组设计下列方案进行实验,请完成下表:
| 你的一种猜想 | 验证方法 | 现象 | 结论 |
| 金属R的活动性比铁 | 将金属R投入 溶液中 | 金属R表面有黑色的物质析出 | 猜想 (选填“正确”或“错误”) |
(6分)请从下列物质中选择适当的物质填空(填字母编号):
| A.干冰 | B.酒精 | C.硫酸 | D.活性炭 E.石灰石 F.维生素C |
(3)蔬菜中富含的营养物质 ;(4)可作冰箱除味剂的是 ;
(5)医疗上常用的消毒剂 ; (6)用于制造水泥、玻璃的矿石是 。