题目内容
(3分) 向盛有一定质量AgNO3和Cu(NO3)2的混合溶液中的烧杯中逐渐加入Zn粉,并边加边搅拌, 溶液质量与加入Zn的质量关系如图所示。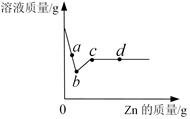
(1)a点的溶液中含有的金属离子有哪些(写离子符号)?
(2) 写出b~c(不包括b点)段反应的化学方程式。
(3)d点的固体中含有几种物质?
(1)Ag+ 、Cu2+、 Zn2+ (2)Zn + Cu(NO3) 2 ="=" Zn(NO3) 2 + Cu
(3)3
解析试题分析:根据金属的活动性顺序,金属Zn、Cu、Ag的活动性顺序是Zn>Cu>Ag,所以在AgNO3和Cu(NO3)2的混合溶液中的烧杯中逐渐加入Zn粉,先发生反应:2AgNO3+Zn==Zn(NO3)2+2Ag,再发生反应:Cu(NO3)2+Zn==Zn(NO3)2+2Cu
(1)结合图像,a点的溶液表示的是第一个反应还在进行,所以此时溶液中含有的金属离子有Ag+ 、Cu2+、 Zn2+
(2)b~c(不包括b点)段表示的是发生第二个反应,化学方程式为:Zn + Cu(NO3) 2 ="=" Zn(NO3) 2 +Cu(3)到了C点表示2个反应都完全发生,自然c~d表示所加的Zn过量,所以d点的固体中含有被置 换出来的Cu、Ag,还有过量的Zn,共3中物质
考点:金属的活动性顺序

练习册系列答案
相关题目
小明同学为了研究影响铁生锈的因素,进行了如下实验:
| 烧瓶号 | 时间/h 导管中水面上升高度/cm | 0 | 0.5 | 1.0 | 1.5 | 2.0 | 2.5 | 3.0 |
| A瓶 | 盛干燥的细铁丝 | 0 | 0 | 0 | 0 | 0 | 0 | 0 |
| B瓶 | 盛浸过食盐水的细铁丝 | 0 | 0.4 | 1.2 | 3.4 | 5.6 | 7.6 | 9.8 |
| C瓶 | 盛浸过清水的细铁丝 | 0 | 0 | 0 | 0.3 | 0.8 | 2.0 | 3.5 |
| D瓶 | 盛完全浸没在食盐水中的细铁丝 | 0 | 0 | 0 | 0 | 0 | 0 | 0 |
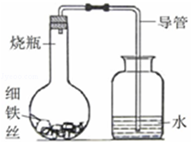
请回答:
(1)以上实验中,铁生锈的速率最大的是 (填烧瓶号)。
(2)导管中水面上升的原因是 。
(3)以上实验说明,影响铁生锈的因素是 。
(4)为了防止钢铁锈蚀,人们常采用在其面涂刷矿物油或镀上其他金属等覆盖保护膜的方法,这些方法的共同原理是 。