题目内容
【题目】工业生产体现了化学的价值,CuCl2 是一种广泛用于生产颜料、木材防腐剂等的化工产品。工业上以辉铜矿(主要含有Cu2S、Fe2O3 及一些不溶性杂质)为原料制备 CuCl22H2O晶体的工艺流程如下:
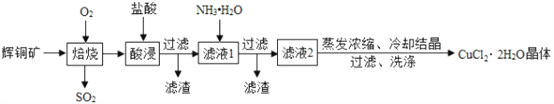
请回答下列问题:
(1)高温焙烧时有黑色氧化铜生成,反应的化学方程式为________。
(2)为加快反应速率,以下措施不能达到目的的是_____。
A.延长酸浸时间 B.将辉铜矿粉碎 C.适当增加盐酸浓度 D.适当提高酸液温度
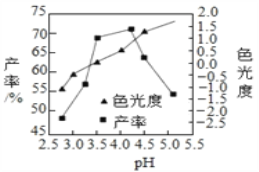
(3)色光度是产品质量指标之一,合格 CuCl22H2O 晶体的色光度范围为﹣0.5~0.5,反应过程溶液pH对产率、色光度的影响如下图所示,综合考虑制备时应控制pH的较合理范围是_______。
(4)测定pH为4.5时不能用pH试纸,可用__________来测量。
【答案】Cu2S+2O2![]() 2CuO+SO2 A 3.5-4.0 pH计(酸度计)
2CuO+SO2 A 3.5-4.0 pH计(酸度计)
【解析】
(1)根据图可知,高温焙烧时是硫化亚铜和氧气反应有黑色氧化铜生成,还生成二氧化硫,反应的化学方程式为Cu2S+2O2![]() 2CuO+SO2;
2CuO+SO2;
(2)A、延长酸浸时间,与速度无关;
B、将辉铜矿粉碎,增大反应物接触面积,加快反应速率;
C、适当增加盐酸浓度,增大了反应物接触的机会,加快反应速率;
D、适当提高酸液温度,分子运动加快,反应速率加快;
(3)色光度是产品质量指标之一,合格CuCl22H2O晶体的色光度范围为-0.5~0.5,根据反应过程溶液pH对产率、色光度的影响图所示,综合考虑制备时应控制pH的较合理范围是 3.4-4;
(4)测定pH为4.5时不能用pH试纸,可用pH计来测量,因为pH试纸只能测整数。

【题目】将一定量的丙醇(CH308)和氧气置于一个封闭的容器中引燃,其反应的化学方程式为: a C3 H8O+ b O2点燃 cCO2+dH2O+eX,测得反应前后各物质的质量如下表:
物 质 | 丙醇 | 氧气 | 水 | 二氧化碳 | X |
反应前质量/g | 6.0 | 12.8 | 0 | 0 | 0 |
反应后质量/g | 0 | 0 | 7.2 | 8.8 | x |
下列判断正确的是
A. 表中x的值为2.8
B. X可能是该反应的催化剂
C. X可能为甲烷
D. 方程式中a:b=1:3
【题目】我们日常生活中,食用的食盐大多来自海水晾晒.海水经蒸发结晶后可获得含有少量泥沙和杂质的粗盐.
(1)为了除去粗盐中含有的少量泥沙,某小组设计了如图所示的实验:在粗盐提纯的过程中,正确的操作顺序是(填序号)______;
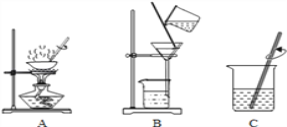
(2)准备过滤器时,为了让折好的滤纸紧贴漏斗壁,应该怎样操作:__________。
(3)实验小组实验数据如下:
称取粗盐/g | 溶解粗盐/g | 剩余粗盐/g | 精盐/g | 精盐产率/% |
5.0 | 3.6 | 1.4 | 2.8 | ? |
该同学的精盐产率为:_______ 。(保留整数)
(4)某同学所得的产率与其他同学比较明显偏低,下列哪些情况导致产率明显偏低______(选填字母序号)
A.溶解时将5.0g粗盐一次全部倒入10mL水中,立即过滤
B.蒸发时有少量液体、固体溅出
C.提纯后的精盐尚未完全干燥就称其质量
(5)粗盐提纯后得到的“精盐”中还含有少量可溶性杂质CaCl2、MgCl2.实验小组的同学设计了以下实验方案来除去可溶性杂质.
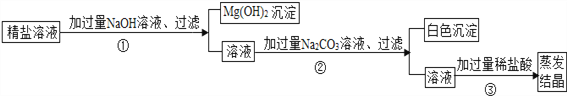
①步骤①的化学方程式为___________。
②步骤②中的白色沉淀为___________。
③步骤③中加稀盐酸是为了除去溶液中_____________。
【题目】水是地球上最普通、最常见的物质之一,不仅江河湖海中含有水,各种生物体也都含有水。下面是关于水的几个小实验。
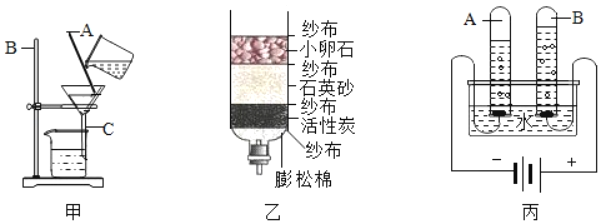
(1)同学们从一水沟中取出了一些浊水,请你参与他们的实验,并完成有关问题。
①甲图中的装置是实验室中过滤水常用的装置,写出下列仪器的名称。
A、_____,B、_____,C、_____。
②若经过甲操作后,所得液体中仍有浑浊,其原因可能是_____(填序号)。
a、漏斗内的滤纸有破损
b、漏斗下端未靠在烧杯内壁
c、漏斗内液面高于滤纸的边缘
(2)如图乙所示是同学们制作的简易净水器完成下列有关问题。
小卵石、石英砂和蓬松棉的作用是_____,活性炭的主要作用是_____。
(3)(提出问题)水的化学式是H2O,它能不能是HO、HO2或其他呢?
(探究课题)水化学式的推导过程。我的假设:水的化学式是H2O或HO或HO2。
(探究准备)精密电解水设备(如图丙所示)
(探究过程)①用精密的电解水设备电解水,同时测定两试管中逸出气体的体积,记录在下表中:
时间/min 体积/mL | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 |
连电源负极的管(A)中气体 | 6 | 12 | 20 | 29 | 39 | 49 | 59 | 69 |
连电源正极的管(B)中气体 | 2 | 4 | 7 | 11 | 16 | 21 | 26 | 31 |
②分析上表中数据可知:电解水时,与电源负极相连的试管中收集到的氢气的体积较多,与电源正极相连的试管中收集到的氧气的体积较少,从第4min开始生成的氢气和氧气的体积比约为_____。
③查阅资料可知:在标准状况下,氢气的密度是0.089g/L,氧气的密度是1.429g/L.由此可对算出生成的氢气和氧气的质量比约为_____。
④利用化合物各元素质量比的算法,设水的化学式为HxOy,根据各元素的质量比=各元素相对原子质量x相应原子个数乘积之比,得出水中氢、氧元素的质量比为_____,所以有_____,解得x:y=_____。
(探究结论)水的化学式是_____。