题目内容
(6分)金属在生产生活中应用广泛。
(1)下列金属制品中,利用金属导热性的是 (填字母序号)。 
A.黄金饰品 B.铁锅 C.铜导线
(2)铁生锈的条件是 ;盐酸可用于金属表面除锈,写出盐酸除去铁锈反应的化学方程式 。
(3)某化学小组用一定量的AgNO3和Zn(NO3)2混合溶液进行了如下图所示实验。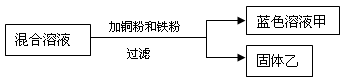
① 向乙中滴加盐酸时 (填“有”或“没有”)气泡产生。
② 甲中一定含有的溶质为 。
(1)B (2)与氧气和水同时接触 Fe2O3+ 6HCl=== 2FeCl3 + 3H2O
(3)① 没有 ② Zn(NO3)2 、Fe(NO3)2、Cu(NO3)2
解析试题分析:(1)性质决定用途,用途反映性质, A、黄金饰品是利用金属光泽,B、铁锅利用导热性,C、铜导线利用导电性
(2)铁生锈的条件是:氧气和水,铁锈的主要成分是氧化铁,所以盐酸除去铁锈反应的化学方程式:Fe2O3+ 6HCl=== 2FeCl3 + 3H2O
(3)①根据金属的活动性:Zn>Fe>Cu>Ag,所以在AgNO3和Zn(NO3)2混合溶液,加入铜粉和铁粉,与Zn(NO3)2不会反应,而与AgNO3都会反应,但由于铁的活动性比铜强,所以是铁反应,然后再是铜与之反应,由于过滤后得到蓝色溶液,说明铁完全被消耗,所以向乙中滴加盐酸时没有气泡产生
②此时甲中一定含有的溶质为:Zn(NO3)2 、Fe(NO3)2、Cu(NO3)2
考点:金属的物理性质,铁生锈的条件金属的活动性

 阅读快车系列答案
阅读快车系列答案小科从某品牌“暖手包”说明书上获悉,该“暖手包”能自动发热,是因为里面有铁粉、活性炭等物质。这些物质对“暖手包”发热有什么作用?小科查阅到下列实验数据:
| 组别 | 时间/min | 铁/g | 活性炭/g | 空气湿度/% | 水/mL | 上升温度/ |
| 1 | 30 | 1 | 0.6 | 70 | 0 | 10.7 |
| 2 | 30 | 1 | 0 | 70 | 0 | 0 |
| 3 | 30 | 0 | 0.6 | 70 | 0 | 0 |
| 4 | 30 | 1 | 0.6 | 40 | 0 | 4.2 |
| 5 | 30 | 1 | 0.6 | 40 | 2 | 11.5 |
(2)分析第1、2、4、5组探究实验可知,“暖手包”的发热还应用了活性炭具有吸附空气中的 的性质。
(4分)化学就在我们身边;化学与我们的生活息息相关。现有八种物质,选择相应物质的字母填空:
| A.活性炭 | B.不锈钢 | C.氮气 | D.纯碱 |
(3) 属于金属材料的是 (4)可做厨房洗涤剂的是