题目内容
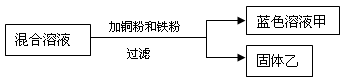
若将一定量的铁粉投入到入一定量只含有Cu(NO3)2、AgNO3的工业废水中,充分反应后过滤,向所得滤渣中滴加稀盐酸,没有气泡产生,则滤渣中一定含有的金属是 ;滤液中一定含有的金属离子是 。
Ag; Fe2+
解析试题分析:依据金属活动性顺序表可得:铁与Cu(NO3)2、AgNO3均能反应,先与AgNO3反应,等硝酸银反应完成后再与硝酸铜反应;因为“滤渣中滴加稀盐酸,没有气泡产生”,铁反应完全,故滤渣中一定不含有铁,一定含有银,可能含有铜;滤液中一定含有硝酸亚铁(新生成),可能有硝酸铜、硝酸银,滤液中一定含有的金属离子是Fe2+。
考点:金属活动性顺序表的应用

练习册系列答案
 天天向上课时同步训练系列答案
天天向上课时同步训练系列答案 阳光课堂同步练习系列答案
阳光课堂同步练习系列答案
相关题目
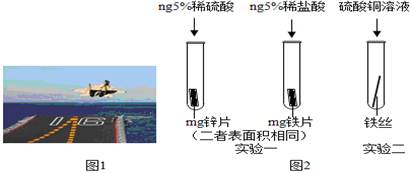
(8分)小强同学分别取溶质质量分数相同的稀盐酸,大小、形状都相同的某种金属X、Al、Cu 进行实验,实验现象记录如下
| | | Al | X | Cu |
| 现象 | 开始时 | 几乎无气泡产生 | 产生气泡速度慢 | 无气泡产生 |
| 一段时间后 | 产生气泡速度快 | 产生气泡速度慢 | 无气泡产生 |
(1)实验开始时,铝表面几乎无气泡产生的原因是__________________ ___;
(2)Cu表面始终无气泡产生的原因是___________ _____;
(3)三种金属的活动性由强到弱的顺序是 ;
(4)如果金属X的活动性比铁弱,且金属X与稀盐酸反应后生成易溶于水的XCl2。向只含有XCl2、CuCl2两种溶质的溶液中加入一定量的铁粉,充分反应后过滤,向滤出的固体中加入稀盐酸,没有气泡产生。则滤液中一定含有的金属阳离子是 (用离子符号表示)。